题目内容
8.下列叙述错误的是( )| A. | Al(OH)3是两性氢氧化物 | |
| B. | 因为Al2O3是金属氧化物,所以它是碱性氧化物 | |
| C. | Al(OH)3能凝聚水中悬浮物,也能吸附色素 | |
| D. | Al(OH)3既溶于NaOH溶液、氨水,又能溶于盐酸 |
分析 A.氢氧化铝能与酸、碱反应生成盐与水,属于两性氢氧化物;
B.氧化铝属于两性氧化物;
C.氢氧化铝形成胶体,表面积很大,具有吸附性;
D.氢氧化铝不能溶于氨水.
解答 解:A.Al(OH)3是既能和强酸反应又能和强碱反应生成盐与水,属于两性氢氧化物,故A正确;
B.氧化铝能与酸反应生成盐与水,能与碱反应生成盐与水,属于两性氧化物,故B错误;
C.Al(OH)3能凝聚水中的悬浮物,常用明矾净水的原理就是由于铝离子水解生成氢氧化铝胶体的缘故,氢氧化铝也能吸附色素,故C正确;
D.氢氧化铝能和强酸以及强碱之间发生反应,但是不能和弱酸以及弱碱之间发生反应,氨水是弱碱,和氢氧化铝不反应,故D错误.
故选BD.
点评 本题考查氧化铝、氢氧化铝的性质与用途等,比较基础,B选项为易错点,注意金属氧化物也可能是酸性氧化物.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
18.下列说法正确的是( )
| A. | 硫完全燃烧生成二氧化硫时,放出的热量为硫的标准燃烧热 | |
| B. | 在101kPa时,1mol碳燃烧所放出的热量为碳的标准燃烧热 | |
| C. | 在101kPa时,由2CO(g)+O2(g)═2CO2(g)△H=-566 kJ•mol-1,可知CO的标准燃烧热为283 kJ•mol-1 | |
| D. | 乙炔的标准燃烧热为1299.6 kJ•mol-1,则2CH2(g)+5O2(g)═4CO2(g)+2H2O(g)反应的△H=-2 599.2 kJ•mol-1 |
19.等物质的量的下列化合物与足量浓盐酸反应,得到氯气物质的量最多的是( )
已知:MnO4-+H++Cl--→Mn2++Cl2↑+H2O(未配平)
ClO3-+H++Cl--→Cl2↑+H2O(未配平)
ClO-+H++Cl--→Cl2↑+H2O(未配平)
已知:MnO4-+H++Cl--→Mn2++Cl2↑+H2O(未配平)
ClO3-+H++Cl--→Cl2↑+H2O(未配平)
ClO-+H++Cl--→Cl2↑+H2O(未配平)
| A. | KClO3 | B. | KMnO4 | C. | MnO2 | D. | Ca(ClO)2 |
3.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 将100mL 0.1mol•L-1的FeCl3溶液滴入沸水中可制得Fe(OH)3胶粒数目为0.0l NA | |
| B. | Na2O2与足量的水反应生成1 molO2,转移电子数目为2 NA | |
| C. | 某密闭容器中有2mo1SO2和1mol O2,在一定条件下充分反应,转移的电子数为4 NA | |
| D. | 18g重水(D2O)所含的电子数为1 NA |
13.在托盘天平右盘上放一个盛有100mL3mol•L-1NaOH溶液的烧杯,左盘上放一个盛有100mL3mol•L-1盐酸的烧杯,调节天平至平衡,然后在两烧杯中各加入等质量2.7g的铝片,反应完全后,则天平可能出现的情况是( )
| A. | 左盘上升 | B. | 右盘下沉 | C. | 仍保持平衡 | D. | 无法判断 |
20.用下列实验装置完成对应实验,能达到实验目的是( )
| A. | 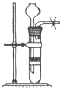 用大理石和盐酸制取CO2 | B. | 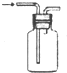 用排气法收集氨气 | ||
| C. | 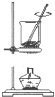 将干海带灼烧成灰 | D. | 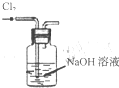 除去Cl2中的HCl |
17.下列物质的检验,其结论一定正确的是( )
| A. | 向某溶液中加入BaCl2溶液,产生白色沉淀,加入HNO3后,白色沉淀不溶解,也无其他现象,说明原溶液中一定含有SO42- | |
| B. | 向某溶液中加盐酸产生无色无味气体,该气体能使澄清的石灰水变浑浊,说明该溶液中一定含有CO32- | |
| C. | 收集氯气时,用湿润的KI淀粉试纸放置于瓶口,观察试纸是否变蓝判断是否收集满 | |
| D. | 某样品的焰色反应呈黄色,则该样品一定是单质钠 |



