题目内容
16.化学与生产、生活息息相关,下列叙述错误的是( )| A. | 铁表而镀铜可以增强其抗腐蚀性 | |
| B. | 用高温催化氧化法去除烃类废气(CxHy):CxHy+(x+$\frac{y}{4}$)O2$→_{高温}^{催化剂}$xCO2+$\frac{y}{2}$H2O | |
| C. | 大量燃烧化石燃料是造成雾霾天气的一种重要因素 | |
| D. | 废旧电池中含有的重金属离子对水和土壤会造成污染,因而不能随意丢弃 |
分析 A.Fe、Cu形成原电池,Fe作负极被腐蚀;
B.烃与氧气反应生成二氧化碳和水;
C.化石燃料燃烧会产生大量烟尘;
D.重金属离子有毒,会污染环境.
解答 解:A.Fe、Cu形成原电池,Fe作负极被腐蚀,所以铁表而镀铜不能增强Fe的抗腐蚀性,故A错误;
B.烃与氧气反应生成二氧化碳和水,所以可以用高温催化氧化法去除烃类废气(CxHy):CxHy+(x+$\frac{y}{4}$)O2$→_{高温}^{催化剂}$xCO2+$\frac{y}{2}$H2O,故B正确;
C.化石燃料燃烧会产生大量烟尘,烟尘是形成雾霾的重要原因,所以大量燃烧化石燃料是造成雾霾天气的一种重要因素,故C正确;
D.废旧电池中含有的重金属离子,重金属离子有毒,会污染环境,所以废旧电池不能随意丢弃,故D正确.
故选A.
点评 本题考查了金属的腐蚀与防护、烃的燃烧、环境保护等,题目难度不大,侧重于化学知识在生产生活中应用的考查,注意对相关知识的积累.

练习册系列答案
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案
相关题目
6.0.1mol/L的NH3•H2O溶液中存在平衡:NH3•H2O?NH4++OH-,下列说法正确的是( )
| A. | 加水时,平衡向逆反应方向移动 | |
| B. | 加入少量氢氧化钠固体,溶液中c(OH-)减小 | |
| C. | 通入少量HCl气体,平衡向正反应方向移动 | |
| D. | 加入少量NH4Cl固体,平衡向正反应方向移动 |
7.下列反应原理不符合工业冶炼金属实际情况的是( )
| A. | 2HgO$\frac{\underline{\;\;△\;\;}}{\;}$2Hg+O2↑ | B. | Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | ||
| C. | 2MgO$\frac{\underline{\;电解\;}}{\;}$2Mg+O2↑ | D. | 2Al2O3$\frac{\underline{\;电解\;}}{\;}$4Al+3O2↑ |
1.检验用硫酸亚铁制得的硫酸铁中是否含有硫酸亚铁,可使用的试剂是( )
| A. | NaOH | B. | KSCN | C. | KMnO4 | D. | 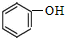 |
5.如图所示与对应叙述相符的是( )
| A. | 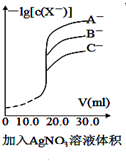 用硝酸银溶液滴定等浓度的A-、B-、C-的混合溶液(均可以与Ag+反应生成沉淀),由图可确定首先沉淀的是C- | |
| B. | 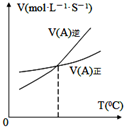 图表示反应中某反应物的正、逆反应速率随温度变化情况,由图可知该反应的正反应是吸热反应 | |
| C. | 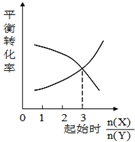 一定条件下,X和Y反应生成Z,由图1推出该反应的方程式可表示为:X+3Y?Z | |
| D. | 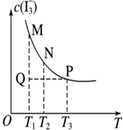 图表示溶液中反应:I2+I-?I3- 平衡c(I3-)随温度变化,反应速度V(正)M<V(逆)N |
14.如图是侯氏制碱法在实验室进行模拟实验的生产流程示意图,则下列叙述正确的是( )


| A. | 第Ⅱ步的离子方程式为Na++NH3+H2O+CO2→NaHCO3↓+NH4+ | |
| B. | 第Ⅲ步得到的晶体是Na2CO3•10H2O | |
| C. | A气体是CO2,B气体是NH3 | |
| D. | 第Ⅳ步操作的过程主要有溶解、蒸发、结晶 |
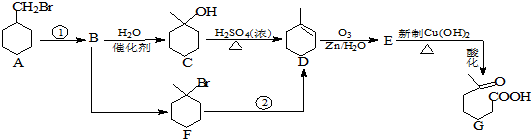
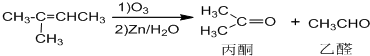
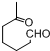 +NaOH+2Cu(OH)2$\stackrel{加热}{→}$
+NaOH+2Cu(OH)2$\stackrel{加热}{→}$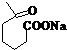 +Cu2O↓+3H2O.
+Cu2O↓+3H2O.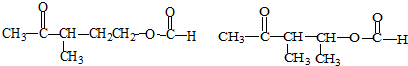
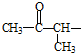 ②属于酯类 ③能发生银镜反应
②属于酯类 ③能发生银镜反应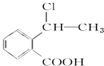 为原料制备
为原料制备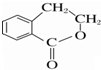 的合成路线流程图(无机试剂任用),并注明反应条件.
的合成路线流程图(无机试剂任用),并注明反应条件.