题目内容
对于可逆反应2A(g)+3B(g)?3C(g),在一定条件下,使一定量A和B气体反应,达到平衡状态时,具有的关系是( )
| A、各物质的量浓度之比为c(A):c(B):c(C)═2:3:3 | ||
B、平衡混合物体积是反应开始前的
| ||
| C、平衡混合物中各物质的量浓度相等 | ||
| D、单位时间内,若消耗了a mol A物质,则同时也消耗了1.5a mol C物质 |
考点:化学平衡状态的判断
专题:化学平衡专题
分析:根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答:
解:A、当体系达平衡状态时,各物质的量浓度之比为c(A):c(B):c(C)可能是也可能不是2:3:3,与各物质的初始浓度及转化率有关,故A错误;
B、达到平衡状态,只是正逆反应速率相等,混合气体装置各组分的体积百分含量不再变化,不一定满足混合气体体积是反应开始前的
,故B错误;
C、当体系达平衡状态时,各物质的浓度可能相等,也可能不等,与各物质的初始浓度及转化率有关,故C错误;
D、单位时间内,若消耗了a mol A物质等效于生成1.5a mol C,则同时也消耗了1.5a mol C物质,故D正确;
故选D.
B、达到平衡状态,只是正逆反应速率相等,混合气体装置各组分的体积百分含量不再变化,不一定满足混合气体体积是反应开始前的
| 3 |
| 5 |
C、当体系达平衡状态时,各物质的浓度可能相等,也可能不等,与各物质的初始浓度及转化率有关,故C错误;
D、单位时间内,若消耗了a mol A物质等效于生成1.5a mol C,则同时也消耗了1.5a mol C物质,故D正确;
故选D.
点评:本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
相关题目
 如图装置可处理乙醛废水,乙醛在阴、阳极发生反应,分别转化为乙醇和乙酸.下列说法正确的是( )
如图装置可处理乙醛废水,乙醛在阴、阳极发生反应,分别转化为乙醇和乙酸.下列说法正确的是( )| A、b电极为正极 |
| B、电解过程中,阴极区Na2SO4的物质的量增大 |
| C、阳极电极反应式为:CH3CHO-2e-+H2O═CH3COOH+2H+ |
| D、电解过程中,两极均有少量气体产生,则阳极产生的是H2 |
下列有关热化学方程式的叙述正确的是( )
| A、2H2(g)+O2(g)═2H2O(g)△H=-483.6 kJ/mol,则氢气的燃烧热为241.8 kJ |
| B、已知C(石墨,s)═C(金刚石,s)△H>0,则金刚石比石墨稳定 |
| C、含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则该反应的热化学方程式为:NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.4 kJ/mol |
| D、已知2C(s)+2O2(g)═2CO2(g)△H1;2C(s)+O2(g)═2CO(g)△H2.则△H1>△H2 |
下列原子序数的原子间不可能形成离子键的是( )
| A、9和12 | B、1和11 |
| C、6和17 | D、3和8 |
下列图示中关于铜电极的连接错误的是( )
A、 稀硫酸 |
B、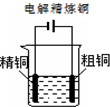 硫酸铜溶液 |
C、 硫酸铜溶液 |
D、 氯化铜溶液 |
下列说法中不正确的是( )
| A、向滴有酚酞的水中加入过量Na202粉末并振荡,溶液由无色变红又变无色 |
| B、向包有Na202粉末的脱脂棉上滴加几滴水,脱脂棉剧烈燃烧起来,说明Na202与H20反应是一个放热反应且有氧气生成 |
| C、Na202与H20反应是一个氧化还原反应,Na202既是氧化剂,又是还原剂 |
| D、Na202与H20反应是一个置换反应,有单质02产生 |
下列氢化物的分子稳定性最好的是( )
| A、HF |
| B、H2O |
| C、NH3 |
| D、CH4 |
 一定温度下,在一定容积的密闭容器中发生如下可逆反应:
一定温度下,在一定容积的密闭容器中发生如下可逆反应: