题目内容
将0.1mol的MnO2和40mL 10mol?L-1的浓盐酸混合后加热,充分反应后,向所得溶液中加入足量的AgNO3溶液.在此过程中:
(1)产生的Cl2在标准状况下的体积V(Cl2)为 (可填写体积范围);
(2)产生的AgCl沉淀的物质的量为 (假设盐酸不挥发,且产生的Cl2的物质的量为a mol).
(1)产生的Cl2在标准状况下的体积V(Cl2)为
(2)产生的AgCl沉淀的物质的量为
考点:化学方程式的有关计算
专题:
分析:(1)发生反应:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,进行过量计算,根据不足量的物质计算生成氯气体积,随反应进行浓盐酸变稀,由于二氧化锰不与稀盐酸反应,实际得到氯气的体积小于计算值;
(2)根据氯原子守恒计算反应后溶液中n(Cl-),发生反应:Cl-+Ag+=AgCl↓,则n(AgCl)=n(Cl-).
| ||
(2)根据氯原子守恒计算反应后溶液中n(Cl-),发生反应:Cl-+Ag+=AgCl↓,则n(AgCl)=n(Cl-).
解答:
解:(1)40mL、10mol/L的浓盐酸中HCl物质的量=0.04L×10mol/L=0.4mol,发生反应:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,由方程式可知0.1mol二氧化锰完全反应消耗HCl为0.1mol×4=0.4mol,等于浓盐酸中含的HCl,若都完全反应则生成氯气为0.1mol,标况下氯气体积=0.1mol×22.4L/mol=2.24L,但随反应进行浓盐酸变稀,由于二氧化锰不与稀盐酸反应,实际得到氯气的体积小于计算值,故0<V(Cl2)<2.24L,
故答案为:0<V(Cl2)<2.24L;
(2)根据氯原子守恒,反应后溶液中n(Cl-)=0.4mol-2amol=(0.4-2a)mol,发生反应:Cl-+Ag+=AgCl↓,则n(AgCl)=n(Cl-)=(0.4-2a)mol,
故答案为:(0.4-2a)mol.
| ||
故答案为:0<V(Cl2)<2.24L;
(2)根据氯原子守恒,反应后溶液中n(Cl-)=0.4mol-2amol=(0.4-2a)mol,发生反应:Cl-+Ag+=AgCl↓,则n(AgCl)=n(Cl-)=(0.4-2a)mol,
故答案为:(0.4-2a)mol.
点评:本题考查化学方程式计算、氧化还原反应计算等,难度不大,(1)注意稀盐酸与二氧化锰不反应,(2)注意利用守恒思想计算.

练习册系列答案
相关题目
在0.1mol/L NH3?H2O 溶液中,下列关系正确的是( )
| A、c(NH3?H2O)>c(OH-)>c(NH4+)>c(H+) |
| B、c(NH4+)>c(NH3?H2O)>c(OH-)>c(H+) |
| C、c(NH3?H2O)>c(NH4+)=c(OH-)>c(H+) |
| D、c(NH3?H2O)>c(NH4+)>c(H+)>c(OH-) |
下列物质久置于空气中会发生相应的变化,其中发生了氧化还原反应的是( )
| A、浓硫酸的体积增大 |
| B、用小刀切割金属钠时,发现切面由银白色变暗 |
| C、澄清的石灰水变浑浊 |
| D、氢氧化钠的表面发生潮解 |
下列晶体性质的比较中,正确的是( )
| A、熔点:SiI4<SiBr4<SiCl4<SiF4 |
| B、沸点:H2S>H2O>HF>NH3 |
| C、熔点:金刚石>晶体硅>晶体锗>硫 |
| D、硬度:金刚石>白磷>冰>水晶 |
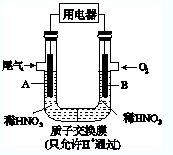 某化学小组构想将汽车尾气(NO、NO2)转化为重要的化工原料HNO3,其原理如图所示,其中A、B为多孔材料.下列说法正确的是( )
某化学小组构想将汽车尾气(NO、NO2)转化为重要的化工原料HNO3,其原理如图所示,其中A、B为多孔材料.下列说法正确的是( )| A、电极A表面反应之一为NO2-e-+H2O═NO3-+2H+ |
| B、电极B附近的c(NO3-)增大 |
| C、电解质溶液中电流的方向由B到A,电子的流向与之相反 |
| D、该电池工作时,每转移4 mol电子,生成22.4LO2 |
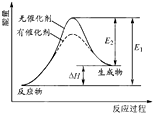 某反应的反应过程中能量的变化如图所示,图中E1表示正反应的活化能,E2表示逆反应的活化能,下列有关叙述正确的是( )
某反应的反应过程中能量的变化如图所示,图中E1表示正反应的活化能,E2表示逆反应的活化能,下列有关叙述正确的是( )| A、该反应为放热反应 |
| B、催化剂能改变该反应的焓变 |
| C、E1也可表示反应物断键需要吸收的总能量 |
| D、△H=E2-E1 |
 标准状况,体积相同的四支试管中分别盛满Cl2、NH3、SO2和NO2,分别倒立在盛有足量水的水槽中(假设进入试管的液体不扩散),光照充分溶解.
标准状况,体积相同的四支试管中分别盛满Cl2、NH3、SO2和NO2,分别倒立在盛有足量水的水槽中(假设进入试管的液体不扩散),光照充分溶解.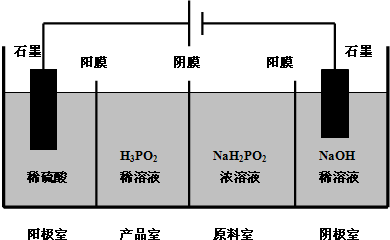 次磷酸(H3PO2)是一种精细磷化工产品,具有较强的还原性.回答下列问题:
次磷酸(H3PO2)是一种精细磷化工产品,具有较强的还原性.回答下列问题: