题目内容
元素周期表共有 个周期、 个族,其中含有 个主族、 个副族.
考点:元素周期表的结构及其应用
专题:
分析:元素周期表共有7个周期、16个族,分别为7个主族、7个副族和1个0族、1个第ⅤⅢ族,以此来解答.
解答:
解:元素周期表有7个横行,则共有7个周期,有18个纵列,共有16个族,分别为7个主族、7个副族和1个0族、1个第ⅤⅢ族,
故答案为:7;16;7;7.
故答案为:7;16;7;7.
点评:本题考查元素周期表的结构,把握周期、族与横行、纵列的关系为解答的关键,注意18个列但分为16个族,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
“复盐”是指含多种简单阳离子和一种酸根离子组成的盐,如KAl(SO4)2.而一种金属离子与多种酸根离子构成的盐则称为“混盐”,如氯化硝酸钙[Ca(NO3)2Cl].下列化合物属于混盐的是( )
| A、Ca2O2Cl4 |
| B、KCl?MgCl2?6H2O |
| C、KMnO4 |
| D、Cu2(OH)2CO3 |
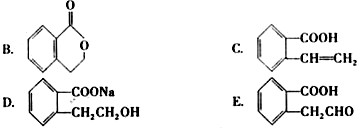
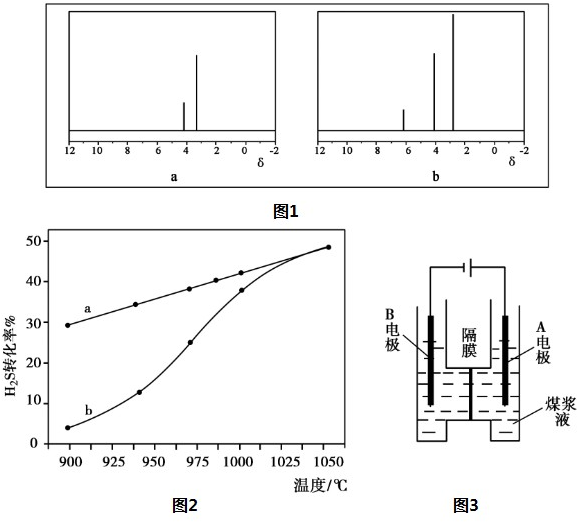
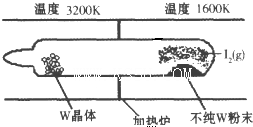 化学反应原理在科研和生产中有广泛应用.
化学反应原理在科研和生产中有广泛应用.