题目内容
HA为酸性略强于醋酸的一元弱酸,在0.1mol/L NaA溶液中,离子浓度关系正确的是( )
| A、c(Na+)>c(A-)>c(H+)>c(OH-) |
| B、c(Na+)>c(A-)>c(OH-)>c(H+) |
| C、c(Na+)+c(OH-)=c(A-)+c(H+) |
| D、c(Na+)+c(H+)=c(A-)+c(OH-) |
考点:离子浓度大小的比较
专题:
分析:NaA为强碱弱酸盐,A-水解导致溶液呈碱性,则c(H+)<c(OH-),A-水解、钠离子不水解,所以c(Na+)>c(A-),A-水解程度较小,则溶液中离子浓度大小顺序为:c(Na+)>c(A-)>c(OH-)>c(H+);溶液中还一定存在电荷守恒:c(Na+)+c(H+)=c(OH-)+c(A-),据此对各选项进行判断.
解答:
解:A.NaA为强碱弱酸盐,A-水解导致溶液呈碱性,则c(H+)<c(OH-),A-水解、钠离子不水解,所以c(Na+)>c(A-),A-水解程度较小,则溶液中离子浓度大小顺序为c(Na+)>c(A-)>c(OH-)>c(H+),故A错误;
B.根据A的分析可知:c(Na+)>c(A-)>c(OH-)>c(H+),故B正确;
C.由于溶液中存在:c(Na+)>c(A-)>c(OH-)>c(H+),则c(Na+)+c(OH-)>c(A-)+c(H+),故C错误;
D.溶液中存在电荷守恒,根据电荷守恒得:c(Na+)+c(H+)=c(OH-)+c(A-),故D正确;
故选BD.
B.根据A的分析可知:c(Na+)>c(A-)>c(OH-)>c(H+),故B正确;
C.由于溶液中存在:c(Na+)>c(A-)>c(OH-)>c(H+),则c(Na+)+c(OH-)>c(A-)+c(H+),故C错误;
D.溶液中存在电荷守恒,根据电荷守恒得:c(Na+)+c(H+)=c(OH-)+c(A-),故D正确;
故选BD.
点评:本题考查了离子浓度大小比较,题目难度中等,明确盐的特点结合“谁强谁显性、谁弱谁水解”来分析解答,注意掌握电荷守恒、物料守恒、盐的水解原理在判断离子浓度大小中的应用方法.

练习册系列答案
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案
相关题目
某溶液可能存在的离子如下:Na+、Ag +、Ba2+、Al3+、AlO2-、CO32-、SO42-、SO32-、S2-.现向该溶液中加入过量的氢溴酸,产生气体和淡黄色沉淀.下列判断正确的是( )
| A、该溶液中一定有Ag+ |
| B、该溶液中可能没有AlO2-、CO32- |
| C、该溶液中一定有Na+ |
| D、该溶液中可能有Ba2+、Al3+ |
在一定浓度的BaCl2溶液中通入SO2气体,未见沉淀生成,若先通入另一种气体,再通入SO2,则可生成白色沉淀.另一种气体不可能是( )
| A、NO2 |
| B、Cl2 |
| C、HCl |
| D、NH3 |
水溶液中能大量共存的一组离子是( )
| A、K+、Cu2+、OH-、HCO3- |
| B、Fe2+、H+、ClO-、SiO32- |
| C、Ca2+、Fe3+、Cl-、CO32- |
| D、Mg2+、NH4+、Br-、SO42- |
 常温下,向10mL 0.1mol?L-1的H2C2O4溶液中逐滴加入0.1mol?L-1 KOH溶液,所得滴定曲线如图所示.下列说法正确的是( )
常温下,向10mL 0.1mol?L-1的H2C2O4溶液中逐滴加入0.1mol?L-1 KOH溶液,所得滴定曲线如图所示.下列说法正确的是( )| A、KHC2O4溶液呈弱碱性 |
| B、B点时:c(K+)>c(HC2O4-)>c(C2O42-)>c(H+)>c(OH-) |
| C、C点时:c(K+)>c(HC2O4-)+c(C2O42-)+c(H2C2O4) |
| D、D点时:c(H+)+c(HC2O4-)+c(H2C2O4)=c(OH-) |
下列实验装置正确且能够达到目的是( )
A、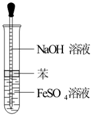 制备Fe(OH)2 |
B、 验证溴与苯发生取代反应 |
C、 测定中和热 |
D、 制备硝基苯 |
下列高分子化合物必须由一种单体缩聚而成的是( )
A、 |
B、 |
C、 |
D、 |
