题目内容
4.为了更好地表示溶液地酸碱性,科学家提出了酸度(AG)的概念,AG=lg$\frac{c({H}^{+})}{c(O{H}^{-})}$,则下列叙述正确的是( )| A. | 中性溶液AG=0 | |
| B. | 常温下0.1mol/L氢氧化钠溶液的AG=12 | |
| C. | 酸性溶液AG<0 | |
| D. | 常温下0.1mol/L的盐酸溶液的AG=13 |
分析 A.中性溶液中c(H+)=c(OH-),AG=lg$\frac{c({H}^{+})}{c(O{H}^{-})}$;
B.常温下0.1mol/L的NaOH溶液中c(OH-)=0.1mol/L,c(H+)=$\frac{{K}_{w}}{c(O{H}^{-})}$=$\frac{1{0}^{-14}mol/L}{0.1mol/L}$=10-13 mol/L,AG=lg$\frac{c({H}^{+})}{c(O{H}^{-})}$;
C.酸性溶液中c(H+)>c(OH-);
D.常温下0.1mol/L的盐酸中c(H+)=0.1mol/L,c(OH-)=$\frac{1{0}^{-14}mol/L}{0.1mol/L}$=10-13 mol/L.
解答 解:A.中性溶液中c(H+)=c(OH-),AG=lg$\frac{c({H}^{+})}{c(O{H}^{-})}$=lg1=0,故A正确;
B.常温下0.1mol/L的NaOH溶液中c(OH-)=0.1mol/L,c(H+)=$\frac{{K}_{w}}{c(O{H}^{-})}$=$\frac{1{0}^{-14}mol/L}{0.1mol/L}$=10-13 mol/L,AG=lg$\frac{c({H}^{+})}{c(O{H}^{-})}$=lg$\frac{1{0}^{-13}}{0.1}$=-12,故B错误;
C.酸性溶液中c(H+)>c(OH-),则AG=lg$\frac{c({H}^{+})}{c(O{H}^{-})}$>lg1=0,故C错误;
D.常温下0.1mol/L的盐酸中c(H+)=0.1mol/L,c(OH-)=$\frac{1{0}^{-14}mol/L}{0.1mol/L}$=10-13 mol/L,则AG=lg$\frac{c({H}^{+})}{c(O{H}^{-})}$=lg$\frac{0.1}{1{0}^{-13}}$=12,故D错误;
故选A.
点评 本题考查pH有关计算,为高频考点,侧重考查学生知识迁移及计算能力,明确酸度计算方法是解本题关键,知道酸中c(OH-)、c(H+)计算方法,题目难度不大.

| A. | Ksp(CaF2)随浓度的变化而变化 | |
| B. | 上述混合体系中有CaF2沉淀生成 | |
| C. | 25℃时,0.1mol/L的HF溶液的pH=l | |
| D. | 上述反应的离子方程式为:Ca2++2F-=CaF2↓ |
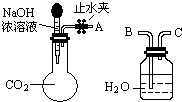 纯碱、烧碱等是重要的化工原料.
纯碱、烧碱等是重要的化工原料.(1)利用如图所示装置可间接证明二氧化碳与烧碱溶液发生了反应.将A与B连接,打开止水夹,将胶头滴管中的液体挤入烧瓶,此时的实验现象是水沿导管由广口瓶进入烧瓶(或:水倒吸进入烧瓶),反应的离子方程式是2OH-+CO2=CO32-+H2O(或CO2+OH-=HCO3-).若其它操作不变,将A与C连接,可观察到的现象是广口瓶中的长导管口有气泡产生.
(2)向100mL2mol/L的NaOH 溶液中通入一定量CO2,结晶,得到9.3g白色固体,该白色固体的组成是NaOH和Na2CO3(写化学式).
设计实验确认该白色固体中存在的阴离子,试完成下列方案.
| 实验操作 | 实验现象 | 结论 |
| ①取少量白色固体于试管中,加足量水溶解,再加足量BaCl2溶液 | 产生白色沉淀 | 有CO32- |
| ②过滤,取2mL滤液于试管中 | ||
| ③滴加酚酞 | 溶液变红 | 有OH- |
| A. | CH4 | B. | C3H8O | C. | C2H4O2 | D. | CH2O |
| A. | 钢铁的吸氧腐蚀和析氢腐蚀的正极反应式均为:Fe-2e-═Fe2+ | |
| B. | 钢铁发生吸氧腐蚀时,负极反应式为:O2+2H2O+4e-═4OH- | |
| C. | 地下钢管连接镁块防腐的方法为“牺牲阳极的阴极保护法” | |
| D. | 钢铁发生吸氧腐蚀时,钢铁制品的质量一定减轻 |
| A. | 1 mol OD-离子含有的质子、中子数均为10NA | |
| B. | 标准状况下,4.48 L己烷含有的分子数为0.2NA | |
| C. | 标准状况下,6.72LNO2与水反应消耗的氧化剂分子数为0.2NA | |
| D. | 丙烯和环丙烷组成的42 g混合气体中氢原子的个数为6NA |
①甲单质能与乙盐的溶液反应并置换出乙
②甲、乙两元素原子的最外层电子数相同,且甲的原子半径小于乙
③甲、乙两短周期元素原子的电子层数相同,且甲的原子序数小于乙
④甲、乙两元素的最高价氧化物水化物的碱性甲大于乙
⑤两单质分别与氯气反应时生成的阳离子,甲失去的电子数比乙多.
| A. | 全部可以 | B. | 仅②可以 | C. | 仅②⑤可以 | D. | ①③④可以 |
| A. | S8转化为S6、S4、S2属于物理变化 | |
| B. | 不论哪种硫分子,完全燃烧时都生成SO3 | |
| C. | S8分子中硫原子的杂化方式是sp3杂化 | |
| D. | 把硫单质在空气中加热到750℃即得S2 |
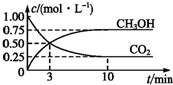 随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍关注,目前工业上有一种方法是用CO2来生产燃料甲醇.为探究反应原理,现进行如下实验:在体积为1L的恒容密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:
随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍关注,目前工业上有一种方法是用CO2来生产燃料甲醇.为探究反应原理,现进行如下实验:在体积为1L的恒容密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应: