题目内容
短周期元素X、Y、Z、Q、R,原子序数依次增大.X、Y两元素最高正价与最低负价之和均为0;Q与X同主族;Z、R分别是地壳中含量最高的非金属元素和金属元素.
由以上某些元素组成的化合物A、B、C、D有如下转化关系:A
B(在水溶液中进行);已知C是溶于水显酸性的气体;D是淡黄色固体.下列叙述错误的是( )
由以上某些元素组成的化合物A、B、C、D有如下转化关系:A
| C |
| D |
A、D的电子式为: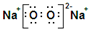 |
| B、X与Y能形成多种化合物,其中既含极性键又含非极性键,且相对分子质量最小的物质的分子式为:C2H2 |
| C、五种元素原子半径由大到小的顺序是:Q>R>Y>Z>X |
| D、A转化为B的离子方程式一定是:2AlO2-+3H2O+CO2→2Al(OH)3↓+CO32- |
考点:原子结构与元素周期律的关系
专题:元素周期律与元素周期表专题
分析:X、Y、Z、Q、R是五种短周期元素,原子序数依次增大.X、Y两元素最高正价与最低负价之和均为0,且Q与X同主族,则X、Q处于ⅠA族,Y处于ⅣA族,故X为氢元素,Q为Na元素,Y为碳元素;Z、R分别是地壳中含量最高的非金属元素和金属元素,则Z为氧元素、R为Al元素,由以上某些元素组成的化合物A、B、C、D有如下转化关系:A
B(在水溶液中进行),其中,C是溶于水显酸性的气体,则C为CO2,D是淡黄色固体,则D为Na2O2,A为NaAlO2,B为Al(OH)3,以此解答该题.
| C |
| D |
解答:
解:X、Y、Z、Q、R是五种短周期元素,原子序数依次增大.X、Y两元素最高正价与最低负价之和均为0,且Q与X同主族,则X、Q处于ⅠA族,Y处于ⅣA族,故X为氢元素,Q为Na元素,Y为碳元素;Z、R分别是地壳中含量最高的非金属元素和金属元素,则Z为氧元素、R为Al元素,由以上某些元素组成的化合物A、B、C、D有如下转化关系:A
B(在水溶液中进行),其中,C是溶于水显酸性的气体,则C为CO2,D是淡黄色固体,则D为Na2O2,A为NaAlO2,B为Al(OH)3,
A.D为Na2O2,电子式为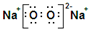 ,故A正确;
,故A正确;
B.C和H形成的化合物中既含极性键又含非极性键,且相对分子质量最小的物质的分子式为C2H2,故B正确;
C.H原子半径最小,同周期自左而右原子半径减小,电子层越多原子半径越多,故原子半径Na>Al>C>O>H,即Q>R>Y>Z>X,故C正确;
D.如二氧化碳过量,则A转化为B的离子方程式可能是:AlO2-+2H2O+CO2=Al(OH)3↓+HCO3-,故D错误.
故选D.
| C |
| D |
A.D为Na2O2,电子式为
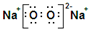 ,故A正确;
,故A正确;B.C和H形成的化合物中既含极性键又含非极性键,且相对分子质量最小的物质的分子式为C2H2,故B正确;
C.H原子半径最小,同周期自左而右原子半径减小,电子层越多原子半径越多,故原子半径Na>Al>C>O>H,即Q>R>Y>Z>X,故C正确;
D.如二氧化碳过量,则A转化为B的离子方程式可能是:AlO2-+2H2O+CO2=Al(OH)3↓+HCO3-,故D错误.
故选D.
点评:本题考查结构性质位置关系应用,推断元素是解题的关键,对学生的理解推理有一定的要求,元素最高正价与最低负价之和均为0,可以为ⅣA族元素,也可以为H元素,中学中较少涉及H元素的负化合价,学生容易忽略,导致无法解答.

练习册系列答案
相关题目
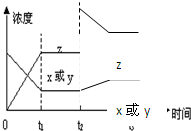 反应x(g)+y(g)?2z(g)△H<0,若反应开始经t1秒后达到平衡,t2秒后由于反应条件的改变使平衡破坏,t3时又达平衡(如图所示),试分析,从t2到t3曲线变化的原因是,t2时刻 ( )
反应x(g)+y(g)?2z(g)△H<0,若反应开始经t1秒后达到平衡,t2秒后由于反应条件的改变使平衡破坏,t3时又达平衡(如图所示),试分析,从t2到t3曲线变化的原因是,t2时刻 ( )| A、减小了x或y的浓度 |
| B、增大了Z的浓度 |
| C、增加了反应体系的压强 |
| D、升高了反应的温度 |
下列说法正确的是( )
| A、氨基酸的晶体主要以内盐形式存在,调节溶液的pH可改变它在水中的溶解度 |
B、2013年4月,国家药监局批准抗H7N9流感的新药帕拉米韦 (结构如图)上市,该药品能与银氨溶液发生银镜反应. (结构如图)上市,该药品能与银氨溶液发生银镜反应. |
C、比例模型 可以表示二氧化碳分子,也可以表示水分子 可以表示二氧化碳分子,也可以表示水分子 |
| D、血红蛋白、牛胰岛素、蚕丝、过氧化氢酶、人造奶油充分水解均可得到氨基酸 |
一定条件将C5H12裂解,最多可以得到烯烃的种数是( )
| A、3种 | B、4种 | C、5种 | D、6种 |
已知某一微粒的核电荷数,则下列一定可以确定的是其( )
| A、质子数 | B、核外电子数 |
| C、电子层数 | D、最外层电子数 |
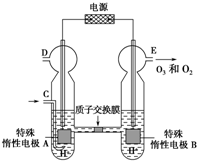 臭氧O3是常用消毒剂,实验室可用电解稀硫酸制备,装置如图(已知溶液中放电顺序:O2>H+).下列说法正确的是( )
臭氧O3是常用消毒剂,实验室可用电解稀硫酸制备,装置如图(已知溶液中放电顺序:O2>H+).下列说法正确的是( )| A、若C处通入O2,电解时溶液中的质子由A极向B极迁移 | ||||
| B、若C处通入O2,A极的电极反应式为:2H++2e-═H2↑ | ||||
C、若C处不通入O2,该制备过程总反应的化学方程式为:3O2
| ||||
D、若C处不通入O2,D、E处分别收集到x L和y L气体(标准状况下),则E处收集的y L气体中O3所占的体积分数为
|
化石燃料仍是目前能源的主体,但已经面临危机,开发新能源是解决能源问题的关键.下列能量转换过程,不涉及化学变化的是( )
| A、利用氢氧燃料电池提供电能 |
| B、利用太阳能分解水制备氢气 |
| C、利用水流驱动涡轮机发电 |
| D、利用植物秸秆为原料生产乙醇燃料 |
下列关于①苯、②乙醇、③乙酸、④葡萄糖等有机物的叙述中,不正确的是( )
| A、一定条件下,可用苯与溴水制取溴苯 |
| B、②、③、④均能与金属钠反应 |
| C、①、②、③均能发生取代反应 |
| D、可以用新制氢氧化铜鉴别①、②、③、④ |
在一定条件下,N2和O2于密闭容器中发生如下反应:2N2(g)+O2(g)?2N2O(g).下列说法能说明该反应达到化学平衡状态的有( )
| A、反应不再进行 |
| B、反应体系中的c(N2)不再发生变化 |
| C、c(N2O)=c(N2) |
| D、N2O的分解速率与生成速率相等 |