题目内容
物质A-J均是中学化学中常见的物质,其相互关系如图所示,已知A、B、C、D、E和F、G、H、I、J中分别含有相同的某一种元素,J物质颜色是红褐色.请填写下列空白:

(1)写出A和OH-反应的离子方程式 ,
(2)B和C反应的离子方程式 ;
(3)写出A和F反应的化学方程式: ;
(4)写出I和O2反应的化学方程式: .暴露在空气中的现象是 .

(1)写出A和OH-反应的离子方程式
(2)B和C反应的离子方程式
(3)写出A和F反应的化学方程式:
(4)写出I和O2反应的化学方程式:
考点:无机物的推断
专题:推断题
分析:A能和酸反应也能和碱反应,说明A具有两性,且B和C能发生反应生成D,D加热生成E,E生成A和氧气,且A到E中都含有同一元素,则这几种物质中都含有铝元素,电解氧化铝生成铝和氧气,则E是Al2O3,A是Al,D是Al(OH)3,B为偏铝酸盐,C是铝盐;
铝和F能在高温下发生反应生成G和氧化铝,则该反应为铝热反应,F为金属氧化物,G是金属单质,G和酸反应生成盐H,H和氢氧根离子反应生成氢氧化物I,I能被氧气氧化生成J,J物质颜色是红褐色,J是Fe(OH)3,J分解生成F,F能被氧气氧化,则I是Fe(OH)2,F是Fe2O3,G是Fe,H为亚铁盐,结合物质的性质分析解答.
铝和F能在高温下发生反应生成G和氧化铝,则该反应为铝热反应,F为金属氧化物,G是金属单质,G和酸反应生成盐H,H和氢氧根离子反应生成氢氧化物I,I能被氧气氧化生成J,J物质颜色是红褐色,J是Fe(OH)3,J分解生成F,F能被氧气氧化,则I是Fe(OH)2,F是Fe2O3,G是Fe,H为亚铁盐,结合物质的性质分析解答.
解答:
解:A能和酸反应也能和碱反应,说明A具有两性,且B和C能发生反应生成D,D加热生成E,E生成A和氧气,且A到E中都含有同一元素,则这几种物质中都含有铝元素,电解氧化铝生成铝和氧气,则E是Al2O3,A是Al,D是Al(OH)3,B为偏铝酸盐,C是铝盐;
铝和F能在高温下发生反应生成G和氧化铝,则该反应为铝热反应,F为金属氧化物,G是金属单质,G和酸反应生成盐H,H和氢氧根离子反应生成氢氧化物I,I能被氧气氧化生成J,J物质颜色是红褐色,J是Fe(OH)3,J分解生成F,F能被氧气氧化,则I是Fe(OH)2,F是Fe2O3,G是Fe,H为亚铁盐,
(1)A和OH-反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(2)B和C反应的离子方程式为Al3++3AlO2-+6H2O=4Al(OH)3↓,
故答案为:Al3++3AlO2-+6H2O=4Al(OH)3↓;
(3)A和F反应的化学方程式为2Al+Fe2O3
2Fe+Al2O3,故答案为:2Al+Fe2O3
2Fe+Al2O3;
(4)I和O2反应的化学方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3,暴露在空气中的现象是白色物质迅速变成灰绿色,最后变成红褐色,
故答案为:4Fe(OH)2+O2+2H2O=4Fe(OH)3;白色物质迅速变成灰绿色,最后变成红褐色.
铝和F能在高温下发生反应生成G和氧化铝,则该反应为铝热反应,F为金属氧化物,G是金属单质,G和酸反应生成盐H,H和氢氧根离子反应生成氢氧化物I,I能被氧气氧化生成J,J物质颜色是红褐色,J是Fe(OH)3,J分解生成F,F能被氧气氧化,则I是Fe(OH)2,F是Fe2O3,G是Fe,H为亚铁盐,
(1)A和OH-反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(2)B和C反应的离子方程式为Al3++3AlO2-+6H2O=4Al(OH)3↓,
故答案为:Al3++3AlO2-+6H2O=4Al(OH)3↓;
(3)A和F反应的化学方程式为2Al+Fe2O3
| ||
| ||
(4)I和O2反应的化学方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3,暴露在空气中的现象是白色物质迅速变成灰绿色,最后变成红褐色,
故答案为:4Fe(OH)2+O2+2H2O=4Fe(OH)3;白色物质迅速变成灰绿色,最后变成红褐色.
点评:本题考查无机物的推断,为高频考点,把握A与酸碱的反应、铝热反应及J为红褐色物质为解答的突破口,侧重Fe、Al及其化合物性质和转化的考查,注重分析能力、应用能力的训练,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在下列物质中,分别加入金属钠,不能产生氢气的是( )
| A、蒸馏水 | B、煤油 |
| C、无水乙醇 | D、苯酚 |
向含Al2(SO4)3和AlCl3的混合溶液中逐滴加入1mol/L Ba(OH)2溶液至过量,加入Ba(OH)2溶液的体积和所得沉淀的物质的量的关系如图,下列说法不正确的是( )
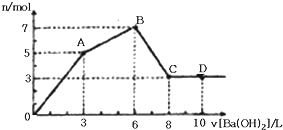

| A、OA段反应的离子方程式为:3Ba2++2Al3++8OH-+3SO42-═3BaSO4↓+2AlO2-+4H2O |
| B、向D点溶液中通入C02气体,立即产生白色沉淀 |
| C、原混合液中c[Al2(SO4)3]:c(AlCl3)═1:2 |
| D、图中C点铝元素存在形式是AlO2- |