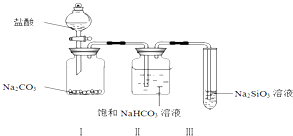
题目内容
5.用一定量的SO2和O2在容积固定的2L密闭容器内发生反应:2SO2+O2?2SO3,如果v(SO2)=0.05mol/(L•min),则2min后SO3的物质的量为( )| A. | 0.2 mol | B. | 0.1 mol | C. | 0.2 mol/L | D. | 0.1 mol/L |
分析 化学反应速率之比等于化学计量数之比,根据v(SO2)可知v(SO3),根据c=$\frac{△c}{△t}$计算2min后SO3的浓度,再根据n=C•V计算2min后SO3的物质的量.
解答 解:如果v(SO2)=0.05mol/(L•min),则v(SO3)=v(SO2)=0.05mol/(L•min),
所以2min后SO3的浓度为0.05mol/(L•min)×2min=0.1mol/L,2min后SO3的物质的量为0.1mol/L×2L=0.2mol,
故选C.
点评 本题考查化学反应速率的计算,侧重于化学反应速率的理解和应用,注意根据化学反应速率之比等于化学计量数之比计算,为解答该题的关键,难度不大.

练习册系列答案
相关题目
16.A、B、C、D四种短周期主族元素的原子序数依次减小;在短周期的主族元素中D的原子半径最大;C原子最外层电子数与电子层数相等;B元素的主要化合价:最高正价+最低负价=4.下列说法正确的是( )
| A. | A、C、D最高价氧化物对应的水化物两两之间能发生反应 | |
| B. | D和A能形成原子个数比为2:1型的离子化合物 | |
| C. | 最高价氧化物对应的水化物的酸性:B>A | |
| D. | C的氧化物是碱性氧化物 |
13.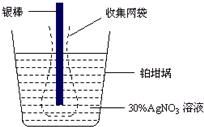 精确测量金属离子在惰性电极上以镀层形式沉积的金属质量,可以确定电解过程中通过电解池的电量.实际测量中常用的银电量计结构如图所示,则下列说法正确的是( )
精确测量金属离子在惰性电极上以镀层形式沉积的金属质量,可以确定电解过程中通过电解池的电量.实际测量中常用的银电量计结构如图所示,则下列说法正确的是( )
 精确测量金属离子在惰性电极上以镀层形式沉积的金属质量,可以确定电解过程中通过电解池的电量.实际测量中常用的银电量计结构如图所示,则下列说法正确的是( )
精确测量金属离子在惰性电极上以镀层形式沉积的金属质量,可以确定电解过程中通过电解池的电量.实际测量中常用的银电量计结构如图所示,则下列说法正确的是( )| A. | 电量计中的银棒应与电源的正极相连,铂棒上发生的电极反应式为:2H++NO3-+e-=NO2↑+H2O | |
| B. | 已知每摩尔电子的电量为96 500 C,若反应进行10分钟,称量电解前后铂坩埚的质量变化值为108.0 mg,则电解过程中的平均电流约为9.65A | |
| C. | 若要测定电解精炼铜时通过的电量,可将银电量计中的银棒与待测电解池的精铜电极相连 | |
| D. | 实验中,为了避免银溶解过程中可能产生的金属颗粒掉进铂坩埚而导致测量误差,常在银电极附近增加一个收集网袋.若没有收集网袋,测量结果会偏低 |
10.下列电子式正确的是( )
| A. | H2O2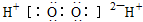 | B. | 羟基: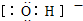 | C. | 甲基: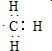 | D. | NH4Cl: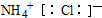 |