题目内容
19.用NA表示阿伏加德罗常数,下列叙述正确的是( )| A. | 2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA | |
| B. | 0.5mol C2H6分子中所含C-H共价键数为2NA | |
| C. | 标准状况下,22.4L乙醇完全燃烧所耗的氧气分子数为3NA | |
| D. | 1mol甲基-CH3所含的电子数为10NA |
分析 A.乙烯和丙烯的最简式为CH2,根据最简式计算含有碳原子数目;
B.分子中含有H原子的数目,根据0.5mol C2H6分子中含有H的物质的量计算;
C.标准状况下,乙醇的状态不是气态;
D.甲基中含有9个电子,1mol甲基中含有9mol电子.
解答 解:A.2.8 g乙烯和丙烯的混合气体中含有2.8g最简式CH2,含有最简式的物质的量为:$\frac{2.8g}{14g/mol}$=0.2mol,则混合物中含有碳原子的物质的量为0.2mol,所含碳原子数为0.2NA,故A正确;
B.0.5mol C2H6分子中含有3molH原子,则所含C-H共价键的物质的量为3mol,含有碳氢键的数目为3NA,故B错误;
C.标况下乙醇不是气体,不能使用标况下的气体摩尔体积计算,故C错误;
D.1mol-CH3含有9mol电子,含有的电子数为9NA,故D错误;
故选A.
点评 本题考查阿伏加德罗常数的综合应用,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确标况下气体摩尔体积的使用条件.

练习册系列答案
相关题目
9.常温下,用0.10mol•L-1的HCl溶液滴定20.00mol•L-1氨水,滴定曲线如图.下列说法正确的是( )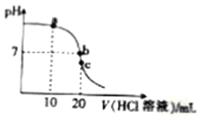

| A. | a点对应的溶液中,c(Cl-)>c(NH4+ )>c(OH- )>c(H+ ) | |
| B. | b点对应的溶液中,c(NH4+)>c(Cl-),c(OH- )=c(H+ ) | |
| C. | c点对应的溶液中,c(H+)=c(NH3•H2O)+c(OH- ) | |
| D. | 滴定过程中可能出现:c(NH4+ )>c(OH- )>c(H+ )>c(Cl-) |
10.下列关于物质分类的说法,正确的是( )
| A. | 碱性氧化物一定是金属氧化物,金属氧化物一定是碱性氧化物 | |
| B. | 由一种元素组成的物质一定是单质,两种元素组成的物质一定是化合物 | |
| C. | 非金属氧化物不一定是酸性氧化物,酸性氧化物不一定都是非金属氧化物 | |
| D. | 硫酸、纯碱、石膏是按酸、碱、盐排列的 |
7.下列离子方程式书写正确的是( )
| A. | Ba(OH)2溶液中加入少量NaHSO4:OH-+H+═H2O | |
| B. | 钠加入水中:Na+2H2O═Na++2OH-+H2↑ | |
| C. | NaOH溶液中通入足量的CO2:OH-+CO2═HCO3- | |
| D. | Al2(SO4)3溶液中加入足量Ba(OH)2溶液:2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ |
14.0.1molAl2(SO4)3与2mol/LNaOH溶液350ml混合,所得沉淀的质量为( )
| A. | 7.8g | B. | 15.6g | C. | 3.9g | D. | 78g |
4.在自然界中只能以化合态存在的元素是( )
| A. | 氮 | B. | 氯 | C. | 硫 | D. | 碳 |
11.下列说法正确的是( )
| A. | 试纸在使用时必须先要湿润 | |
| B. | 任何金属或者它们的化合物在火焰上灼烧都有特殊的焰色反应 | |
| C. | 在配制一定物质的量浓度溶液的定容步骤时,俯视凹液面,所配溶液浓度偏高 | |
| D. | 提纯混有少量硝酸钾的氯化钠,需经过溶解、蒸发浓缩、冷却结晶、过滤、洗涤、干燥等步骤 |
8.对食物的酸、碱性判断正确的是( )
| A. | 柠檬是酸性食物 | B. | 猪肉、牛肉是碱性食物 | ||
| C. | 大多数的蔬菜和水果是碱性食物 | D. | 大米、面粉是碱性食物 |