题目内容
13.下列叙述I和II均正确并有因果关系的是( )| 选项 | 叙述I | 叙述II |
| A | 实验室常用Al2(SO4)3溶液与氨水溶液制备Al(OH)3沉淀 | Al(OH)3不溶于碱 |
| B | NaHCO3为强碱弱酸盐 | NaHCO3溶液显碱性 |
| C | SO2具有氧化性 | SO2可用品红溶液检验 |
| D | 明矾水解产生具有吸附性的胶体 | 明矾可作自来水消毒 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.氢氧化铝是两性氢氧化物溶于强酸强碱,不溶于弱酸弱碱;
B.碳酸氢钠是强碱弱酸盐,溶液中碳酸氢根离子水解程度大于碳酸氢根离子的电离程度;
C.二氧化硫具有中间价态,具有氧化性、还原性,二氧化硫具有漂白性使品红溶液褪色是二氧化硫结合有色物质形成不稳定的无色物质;
D.明矾溶液中铝离子水解生成氢氧化铝胶体具有吸附性,可以净水,不能消毒杀菌;
解答 解:A.氢氧化铝是两性氢氧化物溶于强酸强碱,不溶于弱酸弱碱,实验室常用Al2(SO4)3溶液与氨水溶液制备Al(OH)3沉淀,Al(OH)3能溶于强碱,叙述I正确,叙述II错误,二者无因果关系,故A错误;
B.碳酸氢钠是强碱弱酸盐,溶液中碳酸氢根离子水解程度大于碳酸氢根离子的电离程度溶液显碱性,叙述I和II均正确并有因果关系,故B正确;
C.二氧化硫具有中间价态,具有氧化性、还原性,二氧化硫具有漂白性使品红溶液褪色是二氧化硫结合有色物质形成不稳定的无色物质,不是氧化性,叙述I和II均正确,但无因果关系,故C错误;
D.明矾溶液中铝离子水解生成氢氧化铝胶体具有吸附性,可以净水,不能消毒杀菌,叙述I正确,叙述II错误,无因果关系,故D错误;
故选B.
点评 本题考查了物质性质、反应现象,主要是反应过程中原理的理解应用,注意氢氧化铝的两性和氢氧化铝胶体的吸附作用,题目难度中等.

练习册系列答案
相关题目
3.在以离子键为主的化学键中常含有共价键的成分,两种元素电负性差异越小,其共价键成分越大.下列各对原子形成的化学键中共价键成分最多的是( )
| A. | K与F | B. | Na与F | C. | Al与Cl | D. | Mg与Cl |
1.下图为矿泉水瓶上的部分说明文字,列出了饮用天然水理化指标,这里的钙、钾、钠是指( )

| A. | 原子 | B. | 分子 | C. | 单质 | D. | 元素 |
8.下列有关说法中正确的是( )
| A. | 铁与Cl2、盐酸均能发生反应生成FeCl3 | |
| B. | 加热蒸干并灼烧铁、铝的氯化物溶液,最后均得到金属氧化物 | |
| C. | 等物质的量的Na、Cu、Al与足量氯气反应时消耗氯气一样多 | |
| D. | 常温下铁片、铝片与浓硫酸不能发生化学反应 |
18.能用组成元素的单质直接反应得到的物质是( )
| A. | NO 2 | B. | FeCl2 | C. | SO3 | D. | FeCl3 |
13.在一定温度下的密闭容器中,发生反应:A(s)+2B(g)═2C(g)+D(g),下列说法正确的是( )
| A. | 保持体积不变充入He气,体系压强增大,平衡逆向移动 | |
| B. | 保持压强不变充入He气,因为体系压强不变,所以平衡不移动 | |
| C. | 其它条件不变,向体系中加入A,A的转化率减小,B的转化率增大 | |
| D. | 其它条件不变,改变体积使压强改变,逆方向的速率改变的程度大于正方向 |
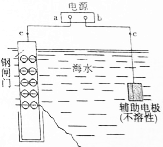 金属是日常生活和工农业生产中广泛使用的材料.恰当的金属防腐方法是延长金属材料使用寿命的前提.
金属是日常生活和工农业生产中广泛使用的材料.恰当的金属防腐方法是延长金属材料使用寿命的前提.