题目内容
下列各组离子在指定溶液中能大量共存的是( )
| A、能使甲基橙变红的溶液中:Na+、K+、AlO2-、SO42- | ||
B、
| ||
| C、加入Al能放出H2 的溶液中:Br-、HSO3 -、SO42-、Fe2+ | ||
| D、由水电离出的c(OH-)=10-11mol?L-1 的溶液中:Na+、K+、Cl-、NO3- |
考点:离子共存问题
专题:离子反应专题
分析:A.使甲基橙变红色的溶液呈酸性,不能大量存在和氢离子反应的离子;
B.
=10-12的水溶液呈强酸性,不能大量存在和氢离子反应的离子;
C.加入Al能放出H2 的溶液为非氧化性酸或强碱溶液,不能大量存在相互反应的离子;
D.由水电离出的c(OH-)=10-11mol?L-1 的溶液呈酸性或碱性,不能大量存在和氢离子或氢氧根离子反应的离子.
B.
| c(OH-) |
| c(H+) |
C.加入Al能放出H2 的溶液为非氧化性酸或强碱溶液,不能大量存在相互反应的离子;
D.由水电离出的c(OH-)=10-11mol?L-1 的溶液呈酸性或碱性,不能大量存在和氢离子或氢氧根离子反应的离子.
解答:
解:A.使甲基橙变红色的溶液呈酸性,偏铝酸根离子和氢离子反应生成氢氧化铝沉淀而不能大量共存,故A错误;
B.
=10-12的水溶液呈强酸性,醋酸根离子和氢离子反应生成弱电解质醋酸,不能大量共存,故B错误;
C.加入Al能放出H2 的溶液为非氧化性酸或强碱溶液,亚硫酸氢根离子和氢离子或氢氧根离子都反应,所以不能大量共存,故C错误;
D.由水电离出的c(OH-)=10-11mol?L-1 的溶液呈酸性或碱性,这几种离子之间不反应且和氢离子或氢氧根离子都不反应,所以能大量共存,故D正确;
故选D.
B.
| c(OH-) |
| c(H+) |
C.加入Al能放出H2 的溶液为非氧化性酸或强碱溶液,亚硫酸氢根离子和氢离子或氢氧根离子都反应,所以不能大量共存,故C错误;
D.由水电离出的c(OH-)=10-11mol?L-1 的溶液呈酸性或碱性,这几种离子之间不反应且和氢离子或氢氧根离子都不反应,所以能大量共存,故D正确;
故选D.
点评:本题考查离子共存,为高考高频点,明确离子反应条件及题中限制性条件是解本题关键,注意C中不能是硝酸,硝酸和铝反应生成氮的化合物,为易错点.

练习册系列答案
 寒假学与练系列答案
寒假学与练系列答案
相关题目
化学与能源开发、环境保护、资源利用等密切相关,下列说法正确的是( )
| A、为提高农作物的产量和质量,应大量使用化肥和农药 |
| B、装饰装修材料中的甲醛、芳香烃及放射性物质都会造成室内污染 |
| C、氯气本身有毒,可以直接杀死水中的细菌和病毒,所以液氯可用于自来水的消毒剂 |
| D、棉、麻、丝、毛及合成纤维完全燃烧都只生成CO2和H2O |
下列说法正确的是( )
| A、用丙酮与盐酸的混合液作展开剂,对Fe3+与Cu2+用纸层析法分离时,Fe3+移动较快 |
| B、阿司匹林制备实验中,将粗产品加入饱和NaOH溶液中以除去水杨酸聚合物 |
| C、用瓷坩锅高温熔融NaOH和Na2CO3的固体混合物 |
| D、标准盐酸滴定待测NaOH溶液,水洗后的酸式滴定管未经标准液润洗,则测定结果偏低 |
常温下,一定量的醋酸与氢氧化钠溶液发生中和反应.下列说法正确的是( )
| A、当溶液中c(CH3COO-)=c (Na+)>c (H+)=c(OH-)时,一定是醋酸过量 |
| B、当溶液中c (CH3COO-)=c (Na+)时,一定是氢氧化钠过量 |
| C、当溶液中c (CH3COO-)=c (Na+)时,醋酸与氢氧化钠恰好完全反应 |
| D、当溶液中c (Na+)>c (CH3COO-)>c (OH-)>c (H+)时,一定是氢氧化钠过量 |
下列说法不正确的是( )
| A、常温下,体积相等、pH=3的盐酸和醋酸,中和NaOH溶液的能力,盐酸小于醋酸 | ||
B、 在一定条件下,将X和Y两种物质按不同的比例放入密闭容器中反应生成Z,平衡后测得X、Y的转化率与率起始时两物质的物质的量之比
| ||
C、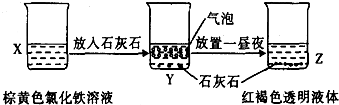 某同学在实验室进行了如图所示的实验,则Y中反应的离子方程式为3CaCO3+2Fe3++3H2O=2Fe(OH)3+3CO2↑+3Ca2+ | ||
D、在25℃时,将amo1?L-l的氨水与0.01 moI?L-1的盐酸等体积混合,反应完全时溶液中c(NH4+)=c(C1-),用含a的代数式表示反应完全时NH3?H2O的电离常数Kb=
|
下列各组物质的性质比较中不正确的是( )
| A、热稳定性:H2S>PH3>SiH4 |
| B、原子半径:Na>Mg |
| C、碱性:NaOH>Mg(OH)2>Al(OH)3 |
| D、结合质子能力:Cl->S2- |