题目内容
有关物质间有下图所示的转化关系.其中:A的浓溶液与单质B在加热时才发生反应①;A的稀溶液与足量B发生反应②.据此填写下列空白:

(1)反应④的现象是 .
(2)写出反应②的离子方程式 .
(3)根据题示信息判断,A的浓溶液和单质B加热时能否产生G,说明理由(写出化学方程式回答): .

(1)反应④的现象是
(2)写出反应②的离子方程式
(3)根据题示信息判断,A的浓溶液和单质B加热时能否产生G,说明理由(写出化学方程式回答):
考点:无机物的推断,常见金属元素的单质及其化合物的综合应用
专题:推断题,几种重要的金属及其化合物
分析:转化关系图中分析判断,单质B和A的浓溶液加热时才能发生反应,说明A为金属在浓酸溶液中发生钝化,加热发生反应,A的稀溶液和B单质反应生成产物与B与浓溶液加热反应产物不同,说明B为变价元素,判断为Fe,A为HNO3,D为Fe(NO3)3,E为NO2,G为Fe(NO3)2,L为Fe(OH)2,K为Fe(OH)3,Q为NaNO3,据此分析回答.
解答:
解:转化关系图中分析判断,单质B和A的浓溶液加热时才能发生反应,说明A为金属在浓酸溶液中发生钝化,加热发生反应,A的稀溶液和B单质反应生成产物与B与浓溶液加热反应产物不同,说明B为变价元素,判断为Fe,A为HNO3,D为Fe(NO3)3,E为NO2,G为Fe(NO3)2,L为Fe(OH)2,K为Fe(OH)3,Q为NaNO3;
(1)反应④是氢氧化亚铁被空气中氧气氧化生成氢氧化铁,反应的现象是,白色沉淀迅速变化为灰绿色,最后变化为红褐色沉淀;
故答案为:白色沉淀→灰绿色→红褐色沉淀;
(2)反应②是过量铁和稀硝酸反应生成硝酸亚铁、一氧化氮和水,反应的离子方程式为:3Fe+2NO3-+8H+═3Fe2++2NO↑+4H2O;
故答案为:3Fe+2NO3-+8H+═3Fe2++2NO↑+4H2O;
(3)由反应2HNO3+NO═3NO2+H2O知,结合化学平衡移动原理分析,在浓HNO3中,平衡正向进行不可能生成NO;
故答案为:由反应2HNO3+NO═3NO2+H2O知,在浓HNO3中不可能生成NO.
(1)反应④是氢氧化亚铁被空气中氧气氧化生成氢氧化铁,反应的现象是,白色沉淀迅速变化为灰绿色,最后变化为红褐色沉淀;
故答案为:白色沉淀→灰绿色→红褐色沉淀;
(2)反应②是过量铁和稀硝酸反应生成硝酸亚铁、一氧化氮和水,反应的离子方程式为:3Fe+2NO3-+8H+═3Fe2++2NO↑+4H2O;
故答案为:3Fe+2NO3-+8H+═3Fe2++2NO↑+4H2O;
(3)由反应2HNO3+NO═3NO2+H2O知,结合化学平衡移动原理分析,在浓HNO3中,平衡正向进行不可能生成NO;
故答案为:由反应2HNO3+NO═3NO2+H2O知,在浓HNO3中不可能生成NO.
点评:本题考查了无机物转化关系的分析判断,反应条件、反应用量和反应产物特征分析判断,主要是铁、硝酸及其化合物性质的分析判断是解题关键,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
二氧化硫和氯气都有漂白性,现把二者以等物质的量混合,让混合气体通入品红溶液,则其漂白性将( )
| A、和氯气单独通过时相同 |
| B、和二氧化硫单独通过时相同 |
| C、是二者作用效果之和 |
| D、失去漂白性 |
下列5个有机化合物中,能够发生酯化、加成和氧化3种反应的是( )
①CH2=CHCOOH ②CH2=CHCOOCH3 ③CH2=CHCH2OH
④CH3CH2CH2OH .
.
①CH2=CHCOOH ②CH2=CHCOOCH3 ③CH2=CHCH2OH
④CH3CH2CH2OH
 .
.| A、①③④ | B、②④⑤ |
| C、①③⑤ | D、①②⑤ |
 立方烷是一种新合成的烃,分子结构是正立方体,如图:
立方烷是一种新合成的烃,分子结构是正立方体,如图: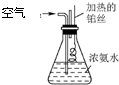 在50mL锥形瓶中盛有20mL浓氨水,向氨水中鼓入空气并迅速将烧红的铂丝伸入瓶中并接近浓氨水的液面.试回答:
在50mL锥形瓶中盛有20mL浓氨水,向氨水中鼓入空气并迅速将烧红的铂丝伸入瓶中并接近浓氨水的液面.试回答:
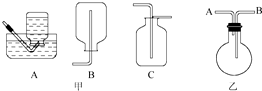 实验室通过加热氯化铵和消石灰来制取氨气.
实验室通过加热氯化铵和消石灰来制取氨气.