题目内容
下列各组中粒子在指定溶液中能大量共存的是( )
| A、0.lmol.L-1氯化铁溶液中Ca2+、Ba2+、Na+、HCO3- | ||
| B、氯水中 H2SO3、K+、SO42-、NH4+ | ||
| C、与镁反应只产生氢气的溶液中 NO3-、C1-、H+、A13+ | ||
D、
|
考点:离子共存问题
专题:离子反应专题
分析:A.离子之间相互促进水解;
B.氯水具有氧化性;
C.与镁反应只产生氢气的溶液,为酸性溶液;
D.
=1.0×1012溶液中,显碱性.
B.氯水具有氧化性;
C.与镁反应只产生氢气的溶液,为酸性溶液;
D.
| c(OH-) |
| c(H+) |
解答:
解:A.Fe3+、HCO3-相互促进水解,不能大量共存,故A错误;
B.氯水具有氧化性,与H2SO3发生氧化还原反应,不能大量共存,故B错误;
C.与镁反应只产生氢气的溶液,为酸性溶液,Mg、NO3-、H+发生氧化还原反应不生成氢气,不大量共存,故C错误;
D.
=1.0×1012溶液中,显碱性,该组离子之间不反应,可大量共存,故D正确;
故选D.
B.氯水具有氧化性,与H2SO3发生氧化还原反应,不能大量共存,故B错误;
C.与镁反应只产生氢气的溶液,为酸性溶液,Mg、NO3-、H+发生氧化还原反应不生成氢气,不大量共存,故C错误;
D.
| c(OH-) |
| c(H+) |
故选D.
点评:本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应、氧化还原反应的离子共存考查,题目难度不大.

练习册系列答案
相关题目
25℃时,20mL硫酸和硝酸的混合溶液,加入足量的氯化钡溶液,充分反应后过滤、洗涤、烘干,可得0.466g沉淀.滤液跟2mol/L NaOH溶液反应,用去10.00mL碱液时恰好中和.下列说法中正确的是( )
| A、原混合液中c(SO42-)=0.2 mol/L |
| B、原混合液中c(NO3-)=0.9 mol/L |
| C、原混合液中pH=0 |
| D、原混合液中由水电离出的c(H+)=0.1 mol/L |
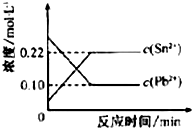 25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq)Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示.下列判断正确的是( )
25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq)Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示.下列判断正确的是( )| A、往平衡体系中加入金属铅后,c(Pb2+)增大 |
| B、往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)变小 |
| C、升高温度,平衡体系中c(Pb2+)增大,说明该反应为吸热反应 |
| D、25℃时,该反应的平衡常数K=2.2 |
Mg-AgCl电池是一种用海水激活的一次电池,在军事上用作电动鱼雷的电源.电池的总反应可表示为:Mg+2AgCl═MgCl2+2Ag下列关于该电池的说法错误的是( )
| A、该电池工作时,正极反应为:2AgCl+2e-═2C1-+2Ag |
| B、该电池的负极材料可以用金属铝代替 |
| C、有24g Mg被氧化时,可还原得到108gAg |
| D、装备该电池的鱼雷在水中行进时,海水作为电解质溶液 |
高铁电池是一种新型可充电电池,该电池长时间保持稳定的放电电压.高铁电池的总反应为:3Zn+2K2FeO4+8H2O
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是( )
| 放电 |
| 充电 |
| A、放电时负极反应为:Zn-2e-+2OH-=Zn(OH)2 |
| B、充电时阳极反应为:Fe(OH)3-3e-+5OH-=FeO42-+4H2O |
| C、放电时每转移1 mol电子,正极有1mol K2FeO4被还原 |
| D、放电时正极附近溶液的pH值升高 |
前18号元素中最外层电子数是次外层电子数一半的元素有( )
| A、1种 | B、2种 | C、3种 | D、4种 |
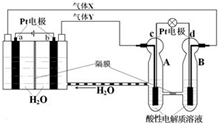 “天宫一号”的供电系统( RFC)是一种将水电解技术与氢氧燃料电池技术相结合的可充放电池.如图所示为RFC工作原理示意图,有关说法正确的是( )
“天宫一号”的供电系统( RFC)是一种将水电解技术与氢氧燃料电池技术相结合的可充放电池.如图所示为RFC工作原理示意图,有关说法正确的是( )| A、当有0.1 mol电子转移时,a极产生1.12 L H2 |
| B、b极上发生的电极反应是:4H2O+4e-=2H2↑+4OH- |
| C、d极上发生的电极反应是:O2+4H++4e-=2H2O |
| D、c极上发生还原反应,B中的H+通过隔膜进入A |
往含有H+、Fe2+、Cu2+、Ag+四种离子的溶液中加入足量镁粉,最先得到的还原产物是( )
| A、H2B |
| B、Fe |
| C、Cu |
| D、Ag |
