��Ŀ����
16����һ���¶��½�������̿��2molˮ���������1L���ܱ������У��������·�Ӧ��C��s��+H2O��g��?CO��g��+H2��g������1���÷�Ӧƽ�ⳣ��K�ı���ʽK=$\frac{c��CO��c��{H}_{2}��}{c��{H}_{2}O��}$
��2����֪��700��ʱ���÷�Ӧ��ƽ�ⳣ��K1=0.6��1 000��ʱ���÷�Ӧ��ƽ�ⳣ��K2Ϊ1.0����÷�ӦΪ�ġ�H��0�����0����0������
��3�����жϸ÷�Ӧ�ﵽ��ѧƽ��״̬��������ABD�������ţ�
A��������������ܶȲ��� B������a mol CO��ͬʱ����a mol H2
C��c��H2O��=c��CO�� D����������ƽ����Է�����������
��4����1 000���£�ijʱ��CO�����ʵ���Ϊ1.0mol�����ʱv��=v�������������=������������ʱH2O��g����ת����Ϊ50%��
���� ��1��ƽ�ⳣ�������������Ũ����֮�����Է�Ӧ���Ũ����֮����ע��CΪ���壻
��2�������¶ȣ�ƽ�ⳣ������˵��ƽ�������ƶ���
��3���ﵽƽ��ʱ�����淴Ӧ������ȣ������ʵ�Ũ�Ȳ��䣬�Դ����������������䣬�Դ��жϣ�
��4����1 000���£�ijʱ��CO�����ʵ���Ϊ1.0mol����ʱK=1����������ʵ���Ũ���ݣ���K��Ƚϣ����ж��Ƿ�ﵽƽ��״̬��������ת���ʣ�
��� �⣺��1��CΪ���壬K=$\frac{c��CO��c��{H}_{2}��}{c��{H}_{2}O��}$���ʴ�Ϊ��K=$\frac{c��CO��c��{H}_{2}��}{c��{H}_{2}O��}$��
��2�������¶ȣ�ƽ�ⳣ������˵��ƽ�������ƶ�����ӦΪ���ȷ�Ӧ��H��0���ʴ�Ϊ����0��
��3��A��̼Ϊ���壬������������ܶȲ��䣬��˵���ﵽƽ��״̬����A��ȷ��
B������a mol CO��ͬʱ����a mol H2��˵�����淴Ӧ������ȣ���˵���ﵽƽ��״̬����B��ȷ��
C��c��H2O��=c��CO��������˵��Ũ�Ȳ��䣬����˵���ﵽƽ��״̬����C����
D����������ƽ����Է����������䣬��˵��������������䣬˵���ﵽƽ��״̬����D��ȷ��
�ʴ�Ϊ��ABD��
��4����1 000���£�ijʱ��CO�����ʵ���Ϊ1.0mol����
C��s��+H2O��g��?CO��g��+H2��g��
��ʼ��mol/L�� 2 0 0
ת����mol/L�� 1 1 1
ƽ�⣨mol/L�� 1 1 1
$\frac{1��1}{1}$=1��˵���ﵽƽ��״̬��
��v��=v����
��ʱH2O��g����ת����Ϊ$\frac{1}{2}��100%$=50%��
�ʴ�Ϊ��=��50%��
���� ���⿼���˻�ѧƽ����йؼ��㣬Ϊ��Ƶ���㣬������ѧ���ķ��������ͼ��������Ŀ��飬�ѶȲ�����ȷ������ʽ�����ǻ�ѧƽ����㳣�õĽ��ⷽ����Ӧ�������գ�

 ��У���˿��ֿ���ϵ�д�
��У���˿��ֿ���ϵ�д� �ƸԴ��ž�ϵ�д�
�ƸԴ��ž�ϵ�д�| A�� | ʳ�׳�ˮ�� | B�� | ʳ�︯�� | ||
| C�� | �ڸ���������������մ� | D�� | ��Һ���������Ȼ�̼��ˮ |
| A�� | Fe3O4�ǻ�ԭ�� | B�� | CO�������� | ||
| C�� | 1mol Fe3O4�õ�6mol���� | D�� | 4molCOʧȥ8mol���� |
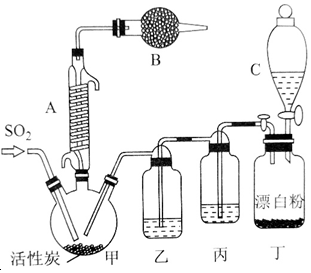 �й���Ϣ���£�������ͨ��������Ϊ��ɫҺ�壬�۵�Ϊ-54.1�棬�е�Ϊ69.1�棬�ڳ�ʪ�����С����̡���100�����Ͽ�ʼ�ֽ⣬���ɶ�����������������ڷ���Ҳ�ᷢ���ֽ⣮�ش��������⣺
�й���Ϣ���£�������ͨ��������Ϊ��ɫҺ�壬�۵�Ϊ-54.1�棬�е�Ϊ69.1�棬�ڳ�ʪ�����С����̡���100�����Ͽ�ʼ�ֽ⣬���ɶ�����������������ڷ���Ҳ�ᷢ���ֽ⣮�ش��������⣺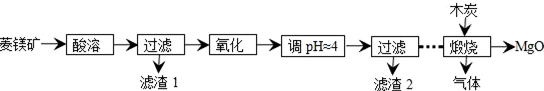

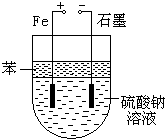 ʵ������NaOH��FeSO4��ȡFe��OH��2ʱ��Fe��OH��2�����ױ���������������ͼ��ʾװ����ȡ�����Եõ��ϴ�����Fe��OH��2��
ʵ������NaOH��FeSO4��ȡFe��OH��2ʱ��Fe��OH��2�����ױ���������������ͼ��ʾװ����ȡ�����Եõ��ϴ�����Fe��OH��2��
 ��
��