题目内容
已知蓄电池在放电时起原电池的作用,充电时起电解池的作用.铅蓄电池在放电和充电时发生的化学反应可用下式表示:
Pb+PbO2+2H2SO4
2PbSO4+2H2O据此判断下列叙述正确的是( )
Pb+PbO2+2H2SO4
| 放电 |
| 充电 |
| A、放电时负极电极反应式为:PbO2+4H++SO42-+2e-=PbSO4+2H2O |
| B、充电时阴极电极反应式为:PbSO4+2e-=Pb+SO42- |
| C、充电时,若要使1mol PbSO4转变为Pb和PbO2,则需要通过2mol电子 |
| D、放电时,H+向负极移动 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:电池放电时负极反应式为:Pb+SO42--2e-=PbSO4,正极反应式为:PbO2+4H++SO42-+2e-=PbSO4+2H2O,电池充电时,阳极上的反应是放电时的正极反应的逆过程,阴极上的反应是放电时负极反应的逆过程,根据电极反应式结合电子守恒来解答.
解答:
解:A、放电时,负极失去电子,则放电时铅蓄电池负极的电极反应为Pb+SO42--2e-=PbSO4,故A错误;
B.充电时,负极与阴极相连,则阴极的电极反应为PbSO4+2e-=Pb+SO42-,故B正确;
C、充电时,若要使1mol PbSO4转变为Pb和PbO2,根据充电时的反应方程式2PbSO4+2H2O=Pb+PbO2+2H2SO4,可得1molPbSO4反应时转移电子数1mol电子,故C错误;
D、放电时,电解质中的阳离子H+向正极移动,在正极得电子,故D错误.
故选B.
B.充电时,负极与阴极相连,则阴极的电极反应为PbSO4+2e-=Pb+SO42-,故B正确;
C、充电时,若要使1mol PbSO4转变为Pb和PbO2,根据充电时的反应方程式2PbSO4+2H2O=Pb+PbO2+2H2SO4,可得1molPbSO4反应时转移电子数1mol电子,故C错误;
D、放电时,电解质中的阳离子H+向正极移动,在正极得电子,故D错误.
故选B.
点评:本题考查铅蓄电池,注意原电池和电解池的分析,明确工作原理及电子守恒是解答本题的关键,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列说法不正确的是( )
| A、除去乙酸乙酯中残留的乙酸,可加过量饱和Na2CO3溶液振荡后,静置分液 |
| B、某烷烃主链4个碳原子数的同分异构体有2种,则与其碳原子个数相同的且主链4个碳原子的单烯烃有4种 |
C、1mol有机物 与NaOH溶液反应,最多消耗5mol NaOH 与NaOH溶液反应,最多消耗5mol NaOH |
D、有机物 分子中所有原子在同一平面内 分子中所有原子在同一平面内 |
下列有关物质的性质或应用的说法中正确的是( )
| A、Si是一种非金属主族元素,其氧化物可用于制作计算机芯片 |
| B、胃穿孔患者胃酸过多时,可服用含Al(OH)3的药片 |
| C、Mg、Fe等金属在一定条件下与水反应都生成H2和对应的氢氧化物 |
| D、铝粉和氧化镁粉末混合,高温能发生铝热反应 |
氢化钙可作为生氢剂,化学方程式是CaH2+2H2O═Ca(OH)2+2H2↑,下列有关叙述正确的是( )
| A、氢化钙被还原 |
| B、水既是氧化剂,又是还原剂 |
| C、H2既是氧化产物,也是还原产物 |
| D、H2O发生氧化反应 |
下列农药不属于有机磷农药的是( )
| A、DDT | B、乐果 |
| C、敌敌畏 | D、敌百虫 |
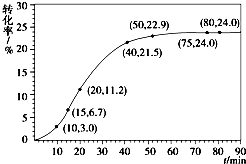 (1)在一定温度下,氧化铁可以与一氧化碳发生下列反应:
(1)在一定温度下,氧化铁可以与一氧化碳发生下列反应: 和一个-Cl,它可能的结构有四种,试写出其中的三种结构简式.
和一个-Cl,它可能的结构有四种,试写出其中的三种结构简式.