题目内容
在0.1mol/LCH3COOH溶液中存在如下电离平衡:CH3COOH
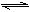 CH3COO-+H+
CH3COO-+H+ 对于该平衡,下列叙述正确的是 ()。
A.加入水,平衡向逆反应方向移动
B.加入少量NaOH固体,平衡向正反应方向移动
C.加入少量0.1mol/LHCl溶液,溶液中c(H+)减小
D.加入少量CH3COONa固体,平衡向正反应方向移动
B
【试题分析】
加入水时,c(CH3COOH)、c(CH3COO-)和c(H+)均减小,使CH3COOH的电离程度增大,平衡向正反应方向移动;加入少量NaOH固体时,中和了H+,使c(H+)减小,平衡向正反应方向移动;加入少量0.1mol/LHCl溶液,尽管平衡向逆反应方向移动,但c(H+)增大;加入少量CH3COONa固体时,c(CH3COO-)增大,平衡向逆反应方向移动。故答案为B。

练习册系列答案
相关题目
在0.5L溶有0.05mol/L NaCl和0.05mol/L CuCl2的溶液中,Cl-的物质的量浓度为( )
| A、0.05mol/L | B、0.1mol/L | C、0.15mol/L | D、0.3mol/L |