题目内容
已知Zn(s)+
O2(g)═ZnO(s)△H=-350kJ/mol,则1g Zn在氧气中燃烧放出的热量约为( )
| 1 |
| 2 |
| A、5.4 kJ |
| B、350 kJ |
| C、3.5 kJ |
| D、8.5 kJ |
考点:有关反应热的计算
专题:化学反应中的能量变化
分析:根据热化学方程式Zn(s)+
O2(g)═ZnO(s)△H=-351kJ/mol,说明1mol锌完全燃烧放出的热量为351kJ,由此计算1gZn在氧气中燃烧放出的热量.
| 1 |
| 2 |
解答:
解:根据热化学方程式Zn(s)+
O2(g)═ZnO(s)△H=-351kJ/mol,说明1mol锌完全燃烧放出的热量为351KJ,则1gZn在氧气中燃烧放出的热量为
=5.4kJ,
故选:A.
| 1 |
| 2 |
| 351kJ |
| 65 |
故选:A.
点评:本题考查热化学方程式的意义和计算,题目难度不大,注意热化学方程式的意义.

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
下列有关煤和石油的叙述中错误的是( )
| A、煤是由有机物和无机物组成的复杂的混合物 |
| B、煤中含有苯和甲苯,可以用先干馏后分馏的方法把它们分离出来 |
| C、石油的催化裂化的目的主要是为了提高轻质油的产量和质量 |
| D、石油的裂解的目的主要是为了获取气态短链不饱和烃 |
图中E表示反应物或生成物的能量,下列说法正确的是( )


| A、图1可表示C+O2→CO2的能量变化过程 |
| B、图1可表示CaCO3→CaO+CO2的能量变化过程 |
| C、图2可表示Mg+2HCl→MgCl2+H2 的能量变化过程 |
| D、图1表示的反应是吸热反应,图2表示的反应是放热反应 |
下列说法中不正确的是( )
①质子数相同的粒子一定属于同一种元素
②同位素的性质几乎相同
③质子数相同电子数也相同的两种粒子,不可能是一种分子或一种离子
④电子数相同的粒子不一定是同一种元素
⑤一种元素只能有一种质量数
⑥某种元素的相对原子质量取整数,就是其质量数.
①质子数相同的粒子一定属于同一种元素
②同位素的性质几乎相同
③质子数相同电子数也相同的两种粒子,不可能是一种分子或一种离子
④电子数相同的粒子不一定是同一种元素
⑤一种元素只能有一种质量数
⑥某种元素的相对原子质量取整数,就是其质量数.
| A、②③⑤⑥ | B、①②④⑤ |
| C、①②⑤⑥ | D、③④⑤⑥ |
在下列化学反应中,既有离子键、极性键、非极性键断裂,又有离子键、极性键、非极性键形成的( )
| A、2Na2O2+2H2O=4NaOH+O2↑ | ||||
| B、Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑ | ||||
| C、Cl2+H2O=HClO+HCl | ||||
D、NH4Cl+NaOH
|
下列有关阿伏伽德罗常数说法正确的是( )
| A、含0.2mol H2SO4的浓硫酸与足量锌反应,生成气体的分子数小于0.1NA |
| B、标况下,22.4L四氯化碳所含分子数大于NA |
| C、0.1mol/L 的AgNO3溶液中,阳离子所带正电荷数目为0.1NA |
| D、电解267g熔融AlCl3,能生成3mol Cl2和54g金属铝 |
在下列有关晶体的叙述中错误的是( )
| A、液态水的密度比冰的密度大,因为水中氢键多 |
| B、原子晶体中,只存在共价键 |
| C、各类晶体中,只有分子晶体才存在分子 |
| D、稀有气体的原子能形成分子晶体 |
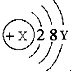 ,试回答:
,试回答: