题目内容
15.下列说法正确的是( )| A. | C4H10有三种同分异构体 | |
| B. | 乙醇、乙二醇、丙三醇互为同系物,同系物之间不可能为同分异物体 | |
| C. | 常温下2S2O(g)=3S(s)+SO2(g)能自发进行,可推断该反应为放热反应 | |
| D. | 因为合金在潮湿的空气中易形成原电池,所以合金耐腐蚀性都较差 |
分析 A、根据碳链异构来解答;
B、结构相似,在分子组成上相差一个或若干个CH2原子团的物质互称为同系物,同系物中官能团的种类与数目要相同;
C、根据反应自发进行的判断依据:△H-△S<0解答;
D、根据不同合金的材料和性能解答.
解答 解:A.C4H10有正丁烷、异丁烷两种同分异构体,故A错误;
B.乙醇、乙二醇与丙三醇所含羟基的个数不同,不为同系物,故B错误;
C.由方程式2S2O(g)═3S(s)+SO2(g)可知该反应△S<0,要使△H-△S<0,必须满足△H<0,故C正确;
D.不是所有的合金耐腐蚀都很差,例如钛合金、铝合金等具有很好的抗腐蚀性能,故D错误;
故选C.
点评 本题考查了金属的腐蚀与防护,同分异构体,同系物,反应方向判据,考查学生对基本知识的掌握程度,题目简单,属于基础题.

练习册系列答案
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案
相关题目
5.合成氨反应为:N2(g)+3H2(g)?2NH3(g).图1表示在一定的温度下此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线.图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响.下列说法正确的是( )
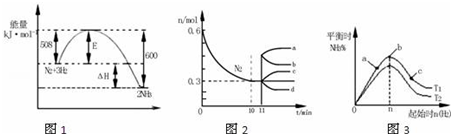

| A. | 由图1可知2NH3(g)?N2(g)+3H2(g)△H=-92kJ•mol-1 | |
| B. | 图2中0~10min内该反应的平均速率v(H2)=0.045mol•L-1•min-1,从11min起其它条件不变,压缩容器的体积为1L,则n(N2)的变化曲线为d | |
| C. | 图3中a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是b点 | |
| D. | 图3中T1和T2表示温度,对应温度下的平衡常数为K1、K2,则:T1>T2,K1>K2 |
6.下列不能用于判断F和Cl的非金属性强弱的事实是( )
| A. | 气态氢化物的稳定性 | B. | 最高价氧化物对应水化物的酸性 | ||
| C. | 单质与氢气反应的难易 | D. | 单质与氢气反应放出热量的多少 |
10.下列对如图两烧杯溶液分析一定正确的是( )


| A. | 甲、乙两烧杯中水电离出OH-浓度:甲<乙 | |
| B. | 分别稀释相同倍数,溶液pH变化:甲=乙 | |
| C. | 相同条件,AgCl(s)在甲中溶解度大于在乙中 | |
| D. | 向乙烧杯加入l0.0mL 0.1mol/L NaOH溶液后一定存在:c(H+)=c(CH3COO-)+c(OH-) |
20.化学与社会、生产、生活紧切相关.下列说法正确的是( )
| A. | 聚乙烯食品袋耐高温加热 | |
| B. | 石英玻璃仪器耐酸碱腐蚀 | |
| C. | 羊毛织物可用强碱性洗涤剂清洗 | |
| D. | 把铅加入锡中制造焊锡的目的是降低熔点 |
7.NA代表阿伏伽德罗常数的值,下列说法不正确的是( )
| A. | 过氧化钠与水反应生成2.24 L O2时转移的电子数为0.2NA | |
| B. | 1 L 14 mol/L硝酸与足量铜反应生成气体分子数小于7NA | |
| C. | 1 L1 mol/L NaHS溶液中H2S、HS-和S2-粒子数之和为NA | |
| D. | 1 mol OH-的电子总数比1 mol-OH的电子总数多NA |
5.向某密闭容器中加人0.3molA、0.1molC和一定量的B三种气体.一定条件下发生反应:aA(g)+bB(g)?cC(g),a、b、c均为正整数,各物质浓度随时间变化如图所示,O~t1min内B的浓度变化没有画出来.下列说法正确的是( )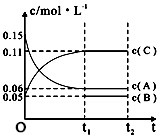

| A. | 若a=3,则b=1,c=2 | |
| B. | t1min时,该反应达到该条件下的反应限度 | |
| C. | 在O~t1min内,用C表示的化学反应速率为0.06mol•L-1 | |
| D. | B的起始浓度等于0.08mol•L-1 |
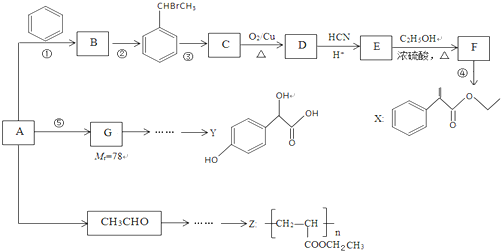
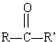 $→_{H+}^{HCN}$
$→_{H+}^{HCN}$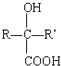 R或R′可以是烃基或氢原子
R或R′可以是烃基或氢原子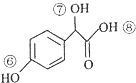 的说法正确的是AD.
的说法正确的是AD. .
.