题目内容
15.加热10.0g碳酸钠和碳酸氢钠的混合物至质量不在变化,剩余固体的质量为8.45g,求(1)混合物中碳酸钠的质量分数.
(2)剩余固体的质量为8.45g与200mL盐酸恰好完全反应.求盐酸的物质的量量浓度.
分析 (1)发生2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,结合反应及差量法计算;
(2)剩余固体为Na2CO3,发生Na2CO3+2HCl=2NaCl+CO2↑+H2O,结合c=$\frac{n}{V}$计算.
解答 解:(1)设碳酸氢钠的质量为x,则
2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O△m
168 106 62
x 10.0g-8.45g
$\frac{162}{x}=\frac{62}{10.0g-8.45g}$,解得x=4.2g,
混合物中碳酸钠的质量分数为$\frac{10.0g-4.2g}{10.0g}$×100%=58%,
答:混合物中碳酸钠的质量分数为58%;
(2)n(NaHCO3)=$\frac{4.2g}{84g/mol}$=0.05mol,加热分解生成的n(Na2CO3)=0.025mol,原混合物中n(Na2CO3)=$\frac{10.0g-4.2g}{106g/mol}$=0.055mol,由Na2CO3+2HCl=2NaCl+CO2↑+H2O可知,n(HCl)=(0.025mol+0.055mol)×2=0.16mol,则盐酸的物质的量量浓度为$\frac{0.16mol}{0.2L}$=0.8mol/L,
答:盐酸的物质的量量浓度为0.8mol/L.
点评 本题考查化学反应的计算,为高频考点,把握发生的反应或差量法计算为解答的关键,侧重分析与计算能力的考查,注意差量法的应用,题目难度不大.

| A. | 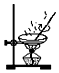 | B. | 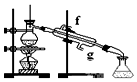 | C. |  | D. | 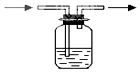 |
| A. | 热交换器 | B. | 沸腾炉 | C. | 吸收塔 | D. | 接触室 |
| A. | Cl-、Br-、CO32- | B. | Br-、CO32-、Cl- | C. | CO32-、Br-、Cl- | D. | Br-、Cl-、CO32- |
| A. | 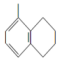 所有碳原子可能在同一平面上 所有碳原子可能在同一平面上 | |
| B. | 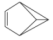 的一氯代物有4种 的一氯代物有4种 | |
| C. | 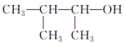 的命名为2,3-二甲基-l-丙醇 的命名为2,3-二甲基-l-丙醇 | |
| D. | 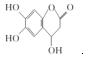 与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H6O6Na4 与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H6O6Na4 |
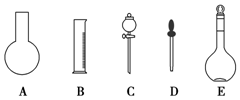 实验室需要0.1mol•L-1 NaOH溶液450mL和0.5mol•L-1硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题:
实验室需要0.1mol•L-1 NaOH溶液450mL和0.5mol•L-1硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题: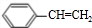 ;.
;.