题目内容
8.下列分子中,所有原子的最外层均为8电子结构的是( )| A. | BeCl2 | B. | H2S | C. | NCl3 | D. | SF3 |
分析 原子的最外层电子数+化合价绝对值=8,则该原子的最外层为8电子结构,以此解答该题.
解答 解:A.铍原子最外层为2电子结构,而不是8电子结构,故A错误;
B.氢原子最外层为2电子结构,而不是8电子结构,故B错误;
C.氮原子和氯原子的最外层电子数+化合价绝对值为8,则原子的最外层均为8电子结构,故C正确;
D.硫原子的最外层电子数+化合价绝对值为9,不是8电子结构,故D错误.
故选C.
点评 本题考查原子核外电子的排布,为高频考点,是对学生原子结构知识的考查,注意规律性的知识在解决选择题中的作用和地位,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
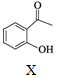
16.合成药物异搏定路线中某一步骤如图:
 +
+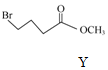 $\stackrel{HaH,DMF}{→}$
$\stackrel{HaH,DMF}{→}$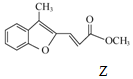 ,下列说法不正确的是( )
,下列说法不正确的是( )
 +
+ $\stackrel{HaH,DMF}{→}$
$\stackrel{HaH,DMF}{→}$ ,下列说法不正确的是( )
,下列说法不正确的是( )| A. | 物质X中所有碳原子可能共平面 | |
| B. | 可用FeCl3溶液鉴别Z中是否含有X | |
| C. | 等物质的量的X、Z分别与H2加成,最多消耗H2的物质的量之比为3:5 | |
| D. | 等物质的量的Y、Z分别与NaOH溶液反应,最多消耗NaOH的物质的量之比为1:1 |
17.除去下列物质中混有的少量杂质(括号内为杂质),所用试剂正确的是( )
| A | Cl2(HCl) | NaOH溶液 |
| B | Fe2O3(Al2O3) | NaOH溶液 |
| C | Na2CO3溶液(NaCl) | AgNO3溶液 |
| D | Na2SO4溶液(Na2CO3) | 稀盐酸 |
| A. | A | B. | B | C. | C | D. | D |
14.常温下,下列各组离子一定可以大量共存的是( )
| A. | 含ClO-的溶液中:H+、K+、Br-、I- | |
| B. | pH=1的溶液中:NH4+、Ba2+、CO32-、NO3- | |
| C. | 在与Al反应能放出H2的溶液中:Mg2+、HCO3-、SO42-、Cl- | |
| D. | 在pH=10的溶液中:Na+、K+、CH3COO-、NO3- |
3.关于中和热的测得实验,下列说法正确的是( )
| A. | 为了使反应进行的更完全,可以使酸或碱适当过量 | |
| B. | 为了使反应均匀进行,可以向酸(碱)中分次加入碱(酸) | |
| C. | 因为中和热为一定值,所以实验结果与所用酸(碱)的用量 和种类均无关 | |
| D. | 测酸溶液的温度后,未冲洗温度计就直接测碱溶液的温度,会使中和热的数值偏大 |
13.乙酸乙酯广泛用于药物、染料、香料等工业,某学习小组设计以下两套装置用乙醇、乙酸和浓硫酸分别制备乙酸乙酯(沸点77.2℃).下列说法不正确的是( )

| A. | 浓硫酸能加快酯化反应速率 | B. | 不断蒸出酯,会降低其产率 | ||
| C. | 装置b比装置a原料损失的少 | D. | 可用分液的方法分离出乙酸乙酯 |
20.下列过程中△H小于零的是( )
| A. | Ba(OH)2与NH4Cl固体混合 | B. | 氯化铵分解得氨气 | ||
| C. | 碳酸钙分解得二氧化碳 | D. | 实验室制备氢气 |
17.下列有关实验操作、现象及结论的叙述正确的是( )
| A. | 用钠可以检验某无水酒精中是否含有水 | |
| B. | 除去甲烷中混有的少量乙烯,可以将混合气体通过酸性KMnO4溶液 | |
| C. | 制取乙酸乙酯时,试剂加入的顺序是:先加入乙醇,后慢慢加入浓硫酸,最后加入乙酸 | |
| D. | 在蔗糖溶液中加入少量稀硫酸,水浴加热后,再加入少量新制的氢氧化铜悬浊液,加热至沸腾,没有砖红色沉淀生成,说明蔗糖没有水解 |
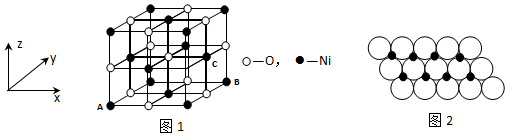
 ,Ni与CO能形成配合物Ni(CO)4,该分子中σ键与π键个数比为1:1.
,Ni与CO能形成配合物Ni(CO)4,该分子中σ键与π键个数比为1:1.