题目内容
11.将10.6g Na2CO3溶于水配成250mL溶液,计算:(1)溶液中溶质的物质的量是多少?
(2)溶液中Na+和CO32-的物质的量浓度.
分析 (1)根据n=$\frac{m}{M}$来解答;
(2)先计算出 Na2CO3的物质的量浓度,然后求出离子的物质的量浓度.
解答 解:(1)溶质的物质的量为$\frac{10.6g}{106g/mol}$=0.1mol,故溶液中溶质的物质的量为0.1mol;答:溶液中溶质的物质的量是0.1mol;
(2)Na2CO3的物质的量浓度为$\frac{0.1mol}{0.25L}$=0.4mol/L,c(Na+)=2c(Na2CO3)=0.8mol/L,c(CO32-)=c(Na2CO3)=0.4mol/L,答:溶液中Na+和CO32-的物质的量浓度分别为0.8mol/L、0.4mol/L.
点评 本题考查物质的量浓度的计算题目,难度不大,注意有关计算公式的运用.

练习册系列答案
相关题目
2.下列实验目的可以达到的是( )
| A. | 漂白粉与浓盐酸反应可制取氯气 | |
| B. | 用FeS与稀硝酸制取硫化氢 | |
| C. | 浓硫酸与碘化钠共热制取碘化氢 | |
| D. | 用浓溴水除去苯中溶有的少量的苯酚 |
19.某元素的原子,L层电子数是M层电子数的2倍,该元素是( )
| A. | Mg | B. | C | C. | Si | D. | S |
16.25℃、101kPa下:
①2Na(s)+$\frac{1}{2}$O2(g)═Na2O(s)△H1=-414kJ/mol
②2Na(s)+O2(g)═Na2O2(s)△H2=-511kJ/mol
下列说法不正确的是( )
①2Na(s)+$\frac{1}{2}$O2(g)═Na2O(s)△H1=-414kJ/mol
②2Na(s)+O2(g)═Na2O2(s)△H2=-511kJ/mol
下列说法不正确的是( )
| A. | ①和②产物的阴阳离子个数比相等,均为1:2 | |
| B. | ①和②生成等物质的量的产物,转移电子数相同 | |
| C. | 常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快 | |
| D. | 25℃、101 kPa下,Na2O2(s)+2Na(s)═2Na2O(s)△H=-317 kJ/mol |
3.从柑桔中炼制萜二烯 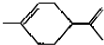 ,下列有关它的推测不正确的是( )
,下列有关它的推测不正确的是( )
 ,下列有关它的推测不正确的是( )
,下列有关它的推测不正确的是( )| A. | 能使酸性高锰酸钾溶液褪色 | |
| B. | 常温下为气态,难溶于水 | |
| C. | 分子式为C10H16 | |
| D. | 与过量的溴的CCl4溶液反应后产物为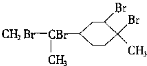 |
20.按酸、碱、盐、氧化物的顺序排列的一组物质是( )
| A. | H2SO4、Na2CO3、NaCl、CuO | B. | H2O、Ca(OH)2、HCl、Na2SO4 | ||
| C. | H2SO4、NaOH、Na2CO3、Fe2O3 | D. | NaOH、H2CO3、NaCl、CO2 |
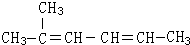 2-甲基-2,4-己二烯.
2-甲基-2,4-己二烯.