题目内容
(1)现有mg某气体,它由双原子分子构成,它的摩尔质量为Mg?mol-1.若阿伏加德罗常数用NA表示,则:
①该气体的物质的量为 mol.
②该气体所含原子总数为 个.
③该气体在标准状况下的体积为 L.
④该气体溶于1L水中(不考虑反应),其溶液中溶质的质量分数为 .
⑤该气体溶于水后形成VL溶液,其溶质的物质的量浓度为 mol?L-1.
(2)检验Cl-先加稀HNO3,再加入 _溶液;检验SO42-先加稀 ,再加入 溶液.(填化学式)
(3)在实验室制取蒸馏水的烧瓶中应放几粒沸石(或碎瓷片),其作用是 ;冷凝管中冷凝水的流向应当是 ;收集蒸馏水时要弃去开始馏出的部分液体,其原因是 .
①该气体的物质的量为
②该气体所含原子总数为
③该气体在标准状况下的体积为
④该气体溶于1L水中(不考虑反应),其溶液中溶质的质量分数为
⑤该气体溶于水后形成VL溶液,其溶质的物质的量浓度为
(2)检验Cl-先加稀HNO3,再加入
(3)在实验室制取蒸馏水的烧瓶中应放几粒沸石(或碎瓷片),其作用是
考点:物质的量的相关计算
专题:计算题
分析:(1)①据n=
来计算;
②根据每个分子中含有的原子数计算总原子数;
③根据V=nVm计算;
④根据质量分数w%=
×100%来计算;
⑤根据c=
来计算;
(2)根据氯离子可以和银离子之间反应生成氯化银沉淀来检验氯离子,根据钡离子和硫酸根离子生成硫酸钡沉淀来检验硫酸根离子;
(3)加入沸石防止加热时烧瓶中液体暴沸;冷凝水应自下而上(从后往前)与蒸气成逆流;收集蒸馏水应除去仪器中含有的自来水.
| m |
| M |
②根据每个分子中含有的原子数计算总原子数;
③根据V=nVm计算;
④根据质量分数w%=
| 溶质质量 |
| 溶液质量 |
⑤根据c=
| n |
| V |
(2)根据氯离子可以和银离子之间反应生成氯化银沉淀来检验氯离子,根据钡离子和硫酸根离子生成硫酸钡沉淀来检验硫酸根离子;
(3)加入沸石防止加热时烧瓶中液体暴沸;冷凝水应自下而上(从后往前)与蒸气成逆流;收集蒸馏水应除去仪器中含有的自来水.
解答:
解:(1)①据n=
,该气体的物质的量为
,故答案为:
;
②因为一个分子中含两个原子,所以含有的原子数为分子数的2倍,即为2×
×NA=
,故答案为:
;
③该体积的体积为
mol×22.4L/mol=
L,故答案为:
;
④根据溶液中溶质的质量分数w%=
×100%=
×100%=
%,故答案为:
%;
⑤根据c=
,所得溶液的物质的量浓度c=
mol/L=
mol/L,故答案为:
;
(2)氯离子可以和银离子之间反应生成氯化银沉淀来检验氯离子,先加稀HNO3,再加入硝酸银溶液即可,钡离子和硫酸根离子生成硫酸钡沉淀来检验硫酸根离子,向溶液中先加入盐酸,排除银离子的干扰,再加入氯化钡来检验硫酸根离子即可,故答案为:AgNO3;HCl;BaCl2;
(3)加入沸石防止加热时烧瓶中液体暴沸;冷凝水应自下而上(从后往前)与蒸气成逆流;收集蒸馏水应除去仪器中含有的自来水,
故答案为:防止液体暴沸;下口进水,上口出水;除去仪器中含有的自来水.
| m |
| M |
| m |
| M |
| m |
| M |
②因为一个分子中含两个原子,所以含有的原子数为分子数的2倍,即为2×
| m |
| M |
| 2mNA |
| M |
| 2mNA |
| M |
③该体积的体积为
| m |
| M |
| 22.4m |
| M |
| 22.4m |
| M |
④根据溶液中溶质的质量分数w%=
| 溶质质量 |
| 溶液质量 |
| m |
| m+1000 |
| 100m |
| m+1000 |
| 100m |
| m+1000 |
⑤根据c=
| n |
| V |
| ||
| V |
| m |
| MV |
| m |
| MV |
(2)氯离子可以和银离子之间反应生成氯化银沉淀来检验氯离子,先加稀HNO3,再加入硝酸银溶液即可,钡离子和硫酸根离子生成硫酸钡沉淀来检验硫酸根离子,向溶液中先加入盐酸,排除银离子的干扰,再加入氯化钡来检验硫酸根离子即可,故答案为:AgNO3;HCl;BaCl2;
(3)加入沸石防止加热时烧瓶中液体暴沸;冷凝水应自下而上(从后往前)与蒸气成逆流;收集蒸馏水应除去仪器中含有的自来水,
故答案为:防止液体暴沸;下口进水,上口出水;除去仪器中含有的自来水.
点评:本题考查常用化学计量数计算、化学实验等,注意对公式的理解,(2)中根据离子的特征反应来检验离子是重点,难度不大.

练习册系列答案
相关题目
下列叙述不正确的是( )
| A、苯与氢气反应属于加成反应 |
| B、苯与硝酸的反应是加成反应 |
| C、苯与液溴生成溴苯 |
| D、苯能够萃取溴水中的溴 |
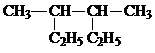 名称:
名称: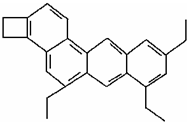
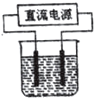 以电解食盐水为基础制取氯气等产品的工业称为“氯碱工业”,它是目前化学工业的重要支柱之一.
以电解食盐水为基础制取氯气等产品的工业称为“氯碱工业”,它是目前化学工业的重要支柱之一.