题目内容
将3molA和3molB气体混合于2L的密闭容器中,发生如下反应:3A(g)+B(g) 2C(g)+2D(g),经5min后,测得D的浓度为0.5mol/L.再经一定时间后达到平衡时,又测得D的浓度为0.6mol/L,试求:
2C(g)+2D(g),经5min后,测得D的浓度为0.5mol/L.再经一定时间后达到平衡时,又测得D的浓度为0.6mol/L,试求:
(1)5min钟内B的平均反应速率?
(2)5min钟时A的浓度?
(3)平衡时B的浓度?
 2C(g)+2D(g),经5min后,测得D的浓度为0.5mol/L.再经一定时间后达到平衡时,又测得D的浓度为0.6mol/L,试求:
2C(g)+2D(g),经5min后,测得D的浓度为0.5mol/L.再经一定时间后达到平衡时,又测得D的浓度为0.6mol/L,试求:(1)5min钟内B的平均反应速率?
(2)5min钟时A的浓度?
(3)平衡时B的浓度?
分析:(1)根据v=
计算v(D),再利用速率之比等于化学计量数之比计算v(B).
(2)结合5min后测得D的浓度为0.5mol/L,根据浓度变化量之比等于化学计量数之比计算△c(A),5min时A的浓度等于A的起始浓度减去△c(A).
(3)结合平衡后测得D的浓度为0.6mol/L,根据浓度变化量之比等于化学计量数之比计算△c(B),平衡时B的浓度等于B的起始浓度减去△c(B).
| △c |
| △t |
(2)结合5min后测得D的浓度为0.5mol/L,根据浓度变化量之比等于化学计量数之比计算△c(A),5min时A的浓度等于A的起始浓度减去△c(A).
(3)结合平衡后测得D的浓度为0.6mol/L,根据浓度变化量之比等于化学计量数之比计算△c(B),平衡时B的浓度等于B的起始浓度减去△c(B).
解答:解:(1)5min钟内,以D表示的平均反应速率v(D)=
=0.1mol/(L﹒min),速率之比等于化学计量数之比,所以v(B)=
v(D)=
×0.1mol/(L﹒min)=0.05mol/(L﹒min).
答:5min钟内B的平均反应速率为0.05mol/(L﹒min).
(2)经5min后测得D的浓度为,即△c(D)=0.6mol/L
浓度变化量之比等于化学计量数之比,所以△c(A)=
×0.5mol/L=0.75mol/L,
5min时A的浓度为
-0.75mol/L=0.75mol/L.
答:5min时A的浓度为0.75mol/L.
(3)平衡后测得D的浓度为0.6mol/L,即△c(D)=0.6mol/L,
浓度变化量之比等于化学计量数之比,所以△c(B)=)=
△c(D)=
×0.6mol/L=0.3mol/L,
所以平衡时B的浓度为
-0.3mol/L=1.5mol/L.
答:平衡时B的浓度为1.5mol/L.
| 0.5mol/L |
| 5min |
| 1 |
| 2 |
| 1 |
| 2 |
答:5min钟内B的平均反应速率为0.05mol/(L﹒min).
(2)经5min后测得D的浓度为,即△c(D)=0.6mol/L
浓度变化量之比等于化学计量数之比,所以△c(A)=
| 3 |
| 2 |
5min时A的浓度为
| 3mol |
| 2L |
答:5min时A的浓度为0.75mol/L.
(3)平衡后测得D的浓度为0.6mol/L,即△c(D)=0.6mol/L,
浓度变化量之比等于化学计量数之比,所以△c(B)=)=
| 1 |
| 2 |
| 1 |
| 2 |
所以平衡时B的浓度为
| 3mol |
| 2L |
答:平衡时B的浓度为1.5mol/L.
点评:考查化学反应速率的有关计算,难度不大,化学反应速率的计算可以用定义法也可以用化学计量数法.

练习册系列答案
相关题目
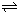 xC(g),达到化学平衡后,C的体积分数为a,假设该反应的条件分别和下列各选项的条件相同,下列判断有不正确的是( )
xC(g),达到化学平衡后,C的体积分数为a,假设该反应的条件分别和下列各选项的条件相同,下列判断有不正确的是( )
 2C(g)+2D(g),经5min后,测得D的浓度为0.5mol/L.再经一定时间后达到平衡时,又测得D的浓度为0.6mol/L,试求:
2C(g)+2D(g),经5min后,测得D的浓度为0.5mol/L.再经一定时间后达到平衡时,又测得D的浓度为0.6mol/L,试求: