题目内容
12.石油资源紧张曾是制约中国发展轿车事业,尤其是制约轿车进入家庭的重要因素.据《扬子晚报》报道,中国宣布将推广“车用乙醇汽油”.(1)写出乙醇完全燃烧的化学方程式C2H5OH+3O2$\stackrel{点燃}{→}$2CO2+3H2O
(2)乙醇燃烧时如果氧气不足,可能还有CO生成.用上图装置确证乙醇燃烧产物有CO、CO2、H2O,应将乙醇燃烧产物依次通过,按气流从左至右顺序填装置编号(可重复)④②①③①.
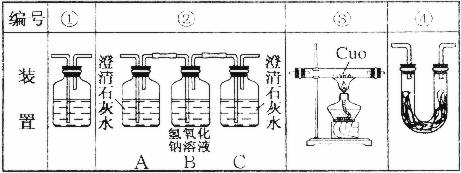
(3)实验时可观察到装置②中A瓶的石灰水变浑浊.A瓶溶液的作用是验证CO2存在;B瓶溶液的作用是除去混合气体中的CO2;C瓶溶液的作用是证明CO2已被除尽.
(4)装置③的作用是CO氧化成CO2,通入③之前装置①的作用是除去水蒸汽(或干燥气体)通入③之后装置①的作用是检验由CO与CuO反应所生成的CO2,从而确定有CO气体.
(5)装置④中所盛的固体药品是无水硫酸铜,它可以确认的产物是H2O.
分析 (1)乙醇完全燃烧生成水、二氧化碳;
(2)④是无水硫酸铜,①是澄清石灰水,乙醇燃烧产物中有CO、CO2和H2O,CO可用热的氧化铜,根据固体颜色的变化;检验二氧化碳可以用澄清石灰水,看是否变浑浊;检验水用无水硫酸铜,看是否变蓝色;三者都有时,应先检验水蒸气的存在,因为在验证二氧化碳、一氧化碳的存在时都需通过溶液,可带出水蒸气;再检验二氧化碳,最后除去二氧化碳后,再根据固体颜色变化和产物检验一氧化碳;
(3)根据二氧化碳可以用澄清石灰水变浑浊,氢氧化钠与二氧化碳反应,能吸收二氧化碳,装置②中A瓶的石灰水变浑浊是检验二氧化碳,B中氢氧化钠是吸收二氧化碳,C中瓶的石灰水是检验二氧化碳是否被除尽;
(4)③和①配合来检验一氧化碳,③是反应装置,①用来检验反应产物;
(5)先通过无水硫酸铜检验水蒸气的存在,因为在验证二氧化碳的存在时需通过溶液,可带出水蒸气.
解答 解:(1)乙醇完全燃烧的化学方程式为C2H5OH+3O2$\stackrel{点燃}{→}$2CO2+3H2O,故答案为:C2H5OH+3O2$\stackrel{点燃}{→}$2CO2+3H2O;
(2)检验乙醇燃烧产物中有CO、CO2和H2O,CO可用热的氧化铜,应先用④检验水蒸气的存在,因为在验证二氧化碳、一氧化碳的存在时都需通过溶液,可带出水蒸气;再用②检验二氧化碳,最后除去二氧化碳后,用①干燥CO,再根据固体颜色变化和产物检验一氧化碳,选择③①,所以顺序为④②①③①,
故答案为:④②①③①;
(3)根据二氧化碳可以用澄清石灰水变浑浊,氢氧化钠与二氧化碳反应,能吸收二氧化碳,装置②中A瓶的石灰水变浑浊是检验二氧化碳,B中氢氧化钠是吸收二氧化碳,C中瓶的石灰水是检验二氧化碳是否被除尽,
故答案为:验证CO2存在;除去混合气体中的CO2;证明CO2已被除尽;
(4)③和①配合来检验一氧化碳,③根据颜色变化判断可能含有一氧化碳,并将一氧化碳氧化成二氧化碳,再用①来进一步确认生成的是二氧化碳,所以③的作用是将CO氧化成CO2;通入③之前装置①的作用是除去水蒸汽(或干燥气体),通入③之后装置①的作用是检验由CO与CuO反应所生成的CO2,从而确定有CO气体,
故答案为:CO氧化成CO2;除去水蒸汽(或干燥气体);检验由CO与CuO反应所生成的CO2,从而确定有CO气体;
(5)先通过无水硫酸铜检验水蒸气的存在,因为在验证二氧化碳、一氧化碳的存在时都需通过溶液,可带出水蒸气,影响水蒸气的确定,
故答案为:无水硫酸铜; H2O.
点评 本题考查性质实验方案的设计,为高频考点,把握物质的性质、实验装置的作用及实验技能为解答的关键,侧重分析与实验能力的考查,注意燃烧产物的检验顺序,题目难度不大.

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案| A. | I2、Br2、Cl2、F2 | B. | Li、Na、K、Rb | C. | F2、Cl2、Br2、I2 | D. | F-、Cl-、Br-、I- |
①a-c=n-m
②元素的原子序数a>b>c>d
③元素非金属性Z>R
④最高价氧化物对应水化物碱性X>Y.
| A. | ①②③④ | B. | ①②③ | C. | ②③ | D. | 只有③ |
| A. | 在高温下,有1 mol Fe与足量的水蒸气反应,转移电子的数目为3NA | |
| B. | 1 mol的羟基与1 mol的氢氧根离子所含电子数均为10NA | |
| C. | 酸性溶液中可能大量存在Na+、ClO?、SO42?、I? | |
| D. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1012的溶液中:NH4+、Al3+、NO3-、Cl-离子组能够大量共存 |
| A. | Fe和Zn | B. | Fe和Ag | C. | Ag和Hg | D. | Mg和Zn |
(2)海水中含有大量的NaCl,盐田法仍是目前海水制盐的主要方法.盐田分为贮水池、蒸发池和结晶池,建盐田必须在BC处建立(填序号).
A.选在离江河入海口比较近的地方B.多风少雨C.潮汐落差大且又平坦空旷的海滩
(3)盐田中所得为粗盐,若想用粗盐制烧碱,需对所用食盐水进行两次精制.第一次精制主要是用沉淀法除去粗盐水中的Ca2+、Mg2+、Fe2+、SO42-等离子,流程如下:
粗盐水$→_{过程Ⅰ}^{过量BaCl_{2}溶液}$$→_{过程Ⅱ}^{过量Na_{2}CO_{3}溶液}$$→_{过程Ⅲ}^{过量NaOH溶液}$$→_{过程Ⅳ}^{过滤}$滤液$→_{调pH}^{盐酸}$第一次精制食盐水
已知:20℃部分沉淀的溶解度(g)如表:
| CaSO4 | CaCO3 | BaSO4 | BaCO3 |
| 2.6×10-2 | 7.8×10-4 | 2.4×10-4 | 1.7×10-3 |
②运用表中数据解释过程I选用BaCl2而不选用CaCl2的原因BaSO4的溶解度比CaSO4的更小,可将SO42-沉淀的更完全.
(4)工业上通常以NaCl、CO2和NH3为原料制取纯碱,请写出第一步制取NaHCO3的化学方程式NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl.
(5)工业制得的纯碱常含有NaCl杂质,用下述方法可以测定样品中NaCl的质量分数.样品中NaCl质量分数的数学表达式为(1-$\frac{106n}{197m}$)×100%.
样品m克$→_{溶解}^{H_{2}O}$溶液$→_{过滤}^{过量BaCl_{2}溶液}$沉淀$→_{洗涤}^{H_{2}O}$$\stackrel{低温烘干、冷却、称量}{→}$固体n克.
| A. | 可能含有丙炔 | B. | 一定没有乙烷 | C. | 一定含有甲烷 | D. | 可能有乙烯 |
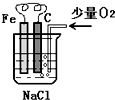 分析图,按要求写出有关反应方程式:
分析图,按要求写出有关反应方程式: