题目内容
5.当一定浓度的醋酸溶液在不同温度下测其H+离子浓度,其结果是( )| A. | 缺少限制条件,无法测定 | B. | H+离子浓度相同 | ||
| C. | 温度低时,H+离子浓度大 | D. | 温度高时,H+离子浓度大 |
分析 醋酸的电离过程属于吸热过程,升高温度促进电离,据此分析.
解答 解:醋酸的电离过程属于吸热过程,升高温度促进电离,当一定浓度的醋酸溶液,在不同温度下测其H+离子浓度,在温度高时,H+离子浓度大,温度低时,H+离子浓度小,故D正确;
故选D.
点评 本题考查了弱电解质的电离以及温度对电离平衡的影响,题目难度不大,注意弱电解质的电离过程为吸热过程.

练习册系列答案
相关题目
20.下列有关说法正确的是( )
| A. | 加入硫酸铜可使锌与稀硫酸的反应速率加快,说明Cu2+具有催化作用 | |
| B. | 根据HA、HB的电离常数的相对大小可以直接判断两种溶液的酸性强弱 | |
| C. | 常温下2S2O(g)═3S(s)+SO2(g)能自发进行,可推断该反应为放热反应 | |
| D. | 将浓硫酸和浓硝酸混合后立即放入铁片,铁片被钝化的效果一定会更好 |
10.用0.01mol•L-1NaOH溶液完全中和pH=3的下列溶液各100mL,需NaOH体积最大的是( )
| A. | 盐酸 | B. | 醋酸 | C. | 硝酸 | D. | 硫酸 |
17.常温下,0.1mol•L-1的HA溶液中$\frac{c(O{H}^{-})}{c({H}^{+})}$=1×10-8,下列叙述中正确的是( )
| A. | 0.01 mol•L-1HA的溶液中c(H+)=1×10-4mol•L-1 | |
| B. | pH=3的HA溶液与pH=11的NaOH溶液等体积混合后所得溶液中c(Na+)>c(A-)>c(OH-)>c(H+) | |
| C. | 浓度均为0.1 mol•L-1的HA溶液和NaA溶液等体积混合后所得溶液显酸性,则 c(OH-)-c(H+)<c(HA)-c(A-) | |
| D. | pH=3的HA溶液与pH=11的NaOH溶液按体积比1:10混合后所得溶液中 c(OH-)+c(A-)═c(H+)+c(Na+) |
15.下列说法或表示方法中正确的是( )
| A. | 等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 | |
| B. | 已知C(s)+$\frac{ax}{0.02}$O2(g)=CO(g)的反应热为110.5kJ/mol,说明碳的燃烧热为110.5kJ | |
| C. | 已知反应X+Y=M+N为放热反应,故不必加热就可发生 | |
| D. | 稀溶液中:H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ•mol-1,若将含0.5 molH2SO4的浓溶液与含1 molNaOH的溶液混合,放出的热量大于57.3KJ |
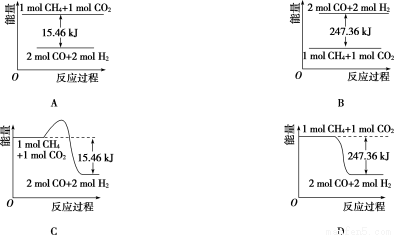
 O、H2)
O、H2)