题目内容
下表为周期表的一部分,其中的编号代表对应的元素.

试填空.
(1)写出上表中元素I的基态原子的电子排布式和价层电子排布图: .元素C、D、E、F的第一电离能由大到小的顺序是 (用元素符号表示).
(2)元素A分别与C、D、E形成最简单的常见化合物分子甲、乙和丙.下列有关叙述不正确的有 .
A.甲、乙和丙分子的空间构型分别为正四面体形、三角锥形、V形
B.甲、乙和丙分子中,中心原子均采取sp3的杂化方式
C.三种分子中键角由大到小的顺序是丙>乙>甲
D.甲、乙和丙分子均为由极性键构成的极性分子
(3)由元素J、C、E组成一种化学式为J(CE)5的配位化合物,该物质常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂.据此可判断:
①该化合物的晶体类型为 .
②该化合物的晶体中存在的作用力有 .
A.离子键 B.极性键 C.非极性键 D.范德华力 E.氢键 F.配位键
③根据共价键理论和等电子体理论分析,CE分子中σ键与π键的数目比为 .
(4)在测定A与F形成的化合物的相对分子质量时,实验测得的值一般高于理论值的主要原因是 .
(5)某些不同族元素的性质也有一定的相似性,如表中元素G与元素B,原因是 .

试填空.
(1)写出上表中元素I的基态原子的电子排布式和价层电子排布图:
(2)元素A分别与C、D、E形成最简单的常见化合物分子甲、乙和丙.下列有关叙述不正确的有
A.甲、乙和丙分子的空间构型分别为正四面体形、三角锥形、V形
B.甲、乙和丙分子中,中心原子均采取sp3的杂化方式
C.三种分子中键角由大到小的顺序是丙>乙>甲
D.甲、乙和丙分子均为由极性键构成的极性分子
(3)由元素J、C、E组成一种化学式为J(CE)5的配位化合物,该物质常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂.据此可判断:
①该化合物的晶体类型为
②该化合物的晶体中存在的作用力有
A.离子键 B.极性键 C.非极性键 D.范德华力 E.氢键 F.配位键
③根据共价键理论和等电子体理论分析,CE分子中σ键与π键的数目比为
(4)在测定A与F形成的化合物的相对分子质量时,实验测得的值一般高于理论值的主要原因是
(5)某些不同族元素的性质也有一定的相似性,如表中元素G与元素B,原因是
考点:元素周期律和元素周期表的综合应用
专题:
分析:由元素在周期表中位置,可知A为氢、B为Be、C为碳、D为氮、E为氧、F为氟、G为Al、H为Cl、I为Cr、J为Fe.
(1)I为Cr,核外电子数目为24,根据能量最低规律书写其核外电子排布式,画出价电子排布图;同周期自左而右元素第一电离能呈增大趋势,当元素原子各轨道处于全满、半满、全空时,能量较低,第一电离能高于同周期相邻元素;
(2)元素A分别与C、D、E形成最简单的常见化合物分子甲、乙和丙分别为CH4、NH3、H2O;
(3)Cr(CO)5为配位化合物,根据其性质可知应为分子晶体,晶体中存在范德华力、配位键,CO中存在极性键;CO与氮气互为等电子体,故CO中C与O原子之间形成三键;
(4)氟化氢气体中存在氢键而相互缔合形成的缔合分子(HF)n;
(5)根据对角线规则分析解答.
(1)I为Cr,核外电子数目为24,根据能量最低规律书写其核外电子排布式,画出价电子排布图;同周期自左而右元素第一电离能呈增大趋势,当元素原子各轨道处于全满、半满、全空时,能量较低,第一电离能高于同周期相邻元素;
(2)元素A分别与C、D、E形成最简单的常见化合物分子甲、乙和丙分别为CH4、NH3、H2O;
(3)Cr(CO)5为配位化合物,根据其性质可知应为分子晶体,晶体中存在范德华力、配位键,CO中存在极性键;CO与氮气互为等电子体,故CO中C与O原子之间形成三键;
(4)氟化氢气体中存在氢键而相互缔合形成的缔合分子(HF)n;
(5)根据对角线规则分析解答.
解答:
解:由元素在周期表中位置,可知A为氢、B为Be、C为碳、D为氮、E为氧、F为氟、G为Al、H为Cl、I为Cr、J为Fe.
(1)I为Cr,核外电子数目为24,其核外电子排布式为1s22s22p63s23p63d54s1,价电子排布图为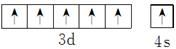 ;同周期自左而右元素第一电离能呈增大趋势,N元素原子各轨道处于全满、半满稳定状态,能量较低,第一电离能高于同周期相邻元素,故第一电离能:F>N>O>C,
;同周期自左而右元素第一电离能呈增大趋势,N元素原子各轨道处于全满、半满稳定状态,能量较低,第一电离能高于同周期相邻元素,故第一电离能:F>N>O>C,
故答案为:1s22s22p63s23p63d54s1、 ;F>N>O>C;
;F>N>O>C;
(2)元素A分别与C、D、E形成最简单的常见化合物分子甲、乙和丙分别为CH4、NH3、H2O,
A.CH4、NH3、H2O的空间构型分别为正四面体形、三角锥形、V形,故A正确;
B.CH4、NH3、H2O中,中心原子均价层电子对数均为4,均采取sp3的杂化方式,故B正确;
C.由于排斥力:孤电子对-孤电子对>孤电子对-成键电子对>成键电子-成键电子,故键角甲烷>氨气>水,故C错误;
D.甲烷是非极性分子,故D错误,
故答案为:CD;
(3)①Cr(CO)5为配位化合物,根据其性质可知应为分子晶体;
②晶体中存在范德华力、配位键,CO中存在极性键;
③CO与氮气互为等电子体,故CO中C与O原子之间形成三键,分子中σ键与π键的数目比为1:2,
故答案为:分子晶体;BDF;1:2;
(4)氟化氢气体中存在氢键而相互缔合形成的缔合分子(HF)n,实验测得的相对分子质量值一般高于理论值,故答案为:氟化氢气体中存在氢键而相互缔合形成的缔合分子(HF)n;
(5)Be与Al在元素周期表中位于对角线的位置,二者性质具有一定的相似性,
故答案为:Be与Al在元素周期表中位于对角线的位置.
(1)I为Cr,核外电子数目为24,其核外电子排布式为1s22s22p63s23p63d54s1,价电子排布图为
 ;同周期自左而右元素第一电离能呈增大趋势,N元素原子各轨道处于全满、半满稳定状态,能量较低,第一电离能高于同周期相邻元素,故第一电离能:F>N>O>C,
;同周期自左而右元素第一电离能呈增大趋势,N元素原子各轨道处于全满、半满稳定状态,能量较低,第一电离能高于同周期相邻元素,故第一电离能:F>N>O>C,故答案为:1s22s22p63s23p63d54s1、
 ;F>N>O>C;
;F>N>O>C;(2)元素A分别与C、D、E形成最简单的常见化合物分子甲、乙和丙分别为CH4、NH3、H2O,
A.CH4、NH3、H2O的空间构型分别为正四面体形、三角锥形、V形,故A正确;
B.CH4、NH3、H2O中,中心原子均价层电子对数均为4,均采取sp3的杂化方式,故B正确;
C.由于排斥力:孤电子对-孤电子对>孤电子对-成键电子对>成键电子-成键电子,故键角甲烷>氨气>水,故C错误;
D.甲烷是非极性分子,故D错误,
故答案为:CD;
(3)①Cr(CO)5为配位化合物,根据其性质可知应为分子晶体;
②晶体中存在范德华力、配位键,CO中存在极性键;
③CO与氮气互为等电子体,故CO中C与O原子之间形成三键,分子中σ键与π键的数目比为1:2,
故答案为:分子晶体;BDF;1:2;
(4)氟化氢气体中存在氢键而相互缔合形成的缔合分子(HF)n,实验测得的相对分子质量值一般高于理论值,故答案为:氟化氢气体中存在氢键而相互缔合形成的缔合分子(HF)n;
(5)Be与Al在元素周期表中位于对角线的位置,二者性质具有一定的相似性,
故答案为:Be与Al在元素周期表中位于对角线的位置.
点评:本题是对物质结构的考查,涉及元素周期表、元素周期律、核外电子排布、分子结构与性质、配合物、氢键等,难度中等,侧重考查学生对知识的应用,需要学生具备扎实的基础.

练习册系列答案
相关题目
下列对沉淀溶解平衡的描述不正确的是( )
| A、用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小 |
| B、物质的溶解度随温度的升高而增加,故物质的溶解都是吸热的 |
| C、除去溶液中的Mg2+,用OH-沉淀Mg2+比用CO32-效果好,说明Mg(OH)2的溶解度比MgCO3大 |
| D、沉淀反应中常加过量的沉淀剂,其目的是使沉淀完全 |
下列说法中正确的是( )
| A、增大反应物浓度,可逆反应正速率增大;减少反应物浓度,可逆反应逆速率增大 |
| B、粗铜精炼时,电解质液中的c(Cu2+)保持不变 |
| C、纯银在空气中久置变黑发生的是电化学腐蚀 |
| D、阴极电保护法是将被保护的金属与外加电源的负极相连 |
如图所示,装置在常温下工作(溶液体积变化忽略不计).闭合K,灯泡发光.下列叙述中不正确的是( )
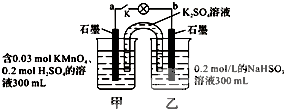

| A、当电路中有1.204×1022个电子转移时,乙烧杯中溶液的C(H+)约为0.1mol?L-1 |
| B、电池工作时,盐桥中的K+移向甲烧杯 |
| C、电池工作时,外电路的电子方向是从a到b |
| D、乙池中的氧化产物为SO42- |
在相同的温度下,100mL 0.01mol?L-1醋酸溶液与10mL 0.1mol?L-1醋酸溶液相比较,下列数值中前者大于后者的是( )
| A、中和时所需氢氧化钠的物质的量 |
| B、H+的物质的量浓度 |
| C、电离平衡常数K |
| D、H+的物质的量 |
气体A、B分别为0.6mol和0.5mol,在0.4L密闭容器中发生反应:3A+B?aC+2D,经5min后,此时C为0.2mol,又知在此反应时间内,D的平均反应速率为0.1mol?(L?min)-1,下列结论正确的是( )
| A、此时,反应混合物总的物质的量为1mol |
| B、B的转化率为50% |
| C、A的平均反应速率为0.1mol?(L?min)-1 |
| D、a值为2 |
下列实验不能达到目的是( )
| A、用溴水除去CH4中混有的C2H4 |
| B、用加热蒸干Na2CO3溶液的方法制备无水Na2CO3固体 |
| C、用分液漏斗分离苯萃取碘水后已分层的有机层和水层 |
| D、加热除去NH4Cl中的少量NaHCO3 |
将标准状况下的a L HCl(气)溶于1L水中,得到的盐酸密度为b g?cm-3,则该盐酸的物质的量浓度是( )
A、
| ||
B、
| ||
C、
| ||
D、
|