题目内容
14.如图虚线框中的装置可用来检验浓硫酸与木炭粉在加热条件下反应产生的所有气体产物,填写下列空白: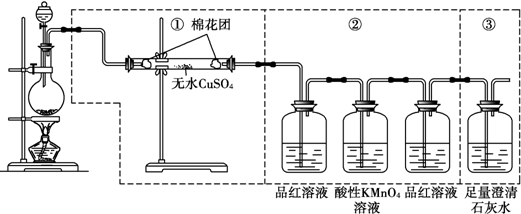
(1)装置中①、②、③可以检验出的物质是①H2O,②SO2,③CO2.
(2)浓硫酸与木炭粉反应的化学方程式:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O.
(3)②中第一瓶品红溶液的作用是检验SO2气体的存在,第二瓶品红溶液的作用是检验SO2是否除尽,酸性KMnO4溶液的作用是氧化除去SO2气体.
(4)证明产生的气体中含有CO2的现象是:②中第二个品红溶液不褪色,③中澄清石灰水变浑浊.
分析 (1)用无水硫酸铜来检验水的生成,用品红检验二氧化硫的生成,用澄清石灰水检验二氧化碳的生成,但是二氧化碳检验之前需要先把二氧化硫除净;(2)碳可以和浓硫酸反应生成二氧化碳、二氧化硫以及水,据此写出反应的化学方程式;
(3)②第一个品红溶液检验二氧化硫的生成,酸性KMnO4溶液除去二氧化硫,再用品红检验二氧化硫是否除尽;
(4)检验二氧化碳气体时必须排除二氧化硫的干扰,即:②中第二个品红溶液不褪色,然后再根据③中澄清石灰水是否变浑浊判断.
解答 解:(1)装置①为无水硫酸铜可以检验水的存在,②品红检验二氧化硫的生成,酸性KMnO4溶液除去二氧化硫,再用品红检验二氧化硫是否除尽,所以②可以检验并除去二氧化硫,③可以检验二氧化碳的存在,故答案为:H2O;SO2;CO2;
(2)碳可以和浓硫酸反应生成二氧化碳、二氧化硫和水,反应的化学方程式为:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O,
故答案为:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O;
(3)因为二氧化碳检验之前需要先把二氧化硫除净,所以②中第一个品红溶液检验二氧化硫的生成,酸性KMnO4溶液除去二氧化硫,再用品红检验二氧化硫是否除尽;故答案为:检验SO2气体的存在;检验SO2是否除尽;氧化除去SO2气体;
(4)二氧化硫和二氧化碳都能够使澄清石灰水变浑浊,当②中第二个品红溶液不褪色,证明二氧化硫已经除尽,若③中澄清石灰水变浑浊,则证明混合气体中存在二氧化碳气体,
故答案为:②中第二个品红溶液不褪色,③中澄清石灰水变浑浊.
点评 本题考查了浓硫酸的性质,题目难度中等,注意掌握C与浓硫酸反应的原理,明确常见气体的性质及检验方法,特别是气体检验的先后顺序.

| A. | 实验室选用高锰酸钾制取氧气 | B. | 氢气在氧气中燃烧生成水 | ||
| C. | 煅烧石灰石制取生石灰 | D. | 用锌粒和盐酸制取氢气 |
| A. | 氯水 | B. | 钠 | C. | 浓硝酸 | D. | 浓盐酸 |
| A. | 升高温度可以提高CO的转化率 | |
| B. | 加入催化剂能提高CO的转化率 | |
| C. | 缩小反应器容积可以使平衡正向移动 | |
| D. | 再充入适量H2,该反应平衡常数的数值会增大 |
 某课外小组利用下列装置,对浓硫酸与乙醇反应的可能产物进行了如下探究.
某课外小组利用下列装置,对浓硫酸与乙醇反应的可能产物进行了如下探究.
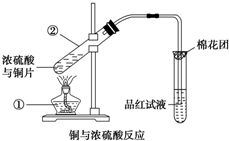 如图是铜与浓硫酸反应的实验装置图,请回答下列问题.
如图是铜与浓硫酸反应的实验装置图,请回答下列问题.