题目内容
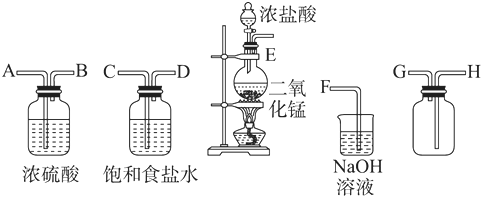
9.下列装置或操作不能达到实验目的是( )| A. |  比较 Cl2、Fe3+、I2的氧化性 | B. |  制取 Fe(OH)2 制取 Fe(OH)2 | ||
| C. | 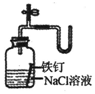 证明铁生锈时空气参加反应 | D. | 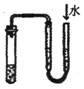 检查装置气密性 |
分析 A.氯气可氧化碘离子、亚铁离子,且先氧化碘离子;
B.Fe与硫酸生成的氢气可排出空气,但氢气很难将硫酸亚铁与NaOH混合;
C.发生吸氧腐蚀;
D.加水,调节液面形成液面差.
解答 解:A.氯气可氧化碘离子、亚铁离子,且氯气少量先氧化碘离子,则可比较 Cl2、Fe3+、I2的氧化性,故A正确;
B.Fe与硫酸生成的氢气可排出空气,但氢气很难将硫酸亚铁与NaOH混合,图中左侧试管中应长导管深入液面下,故B错误;
C.发生吸氧腐蚀,则证明铁生锈时空气参加反应,故C正确;
D.加水,调节液面形成液面差,一段时间液面差不变,可说明气密性良好,故D正确;
故选B.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、物质的制备、电化学腐蚀、气密性检验、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目
19.下列各物质的同分异构体中,能形成顺、反异构体的是( )
| A. | 1,1-二氯乙烯 | B. | 丙烯 | C. | 1-丁烯 | D. | 2-戊烯 |
20.在CO2中,Mg燃烧生成MgO和C.下列说法正确的是( )
| A. | 在该反应条件下,Mg的还原性强于C的还原性 | |
| B. | Mg、MgO中镁元素微粒的半径:r(Mg2+)>r(Mg) | |
| C. | 元素C的单质只存在金刚石和石墨两种同素异形体 | |
| D. | 该反应中化学能全部转化为热能 |
17.一定温度下,容积为2L的甲、乙两固定容积的密闭容器中,发生反应:2SO 2(g)+O 2(g)?2SO 3(g).达平衡时测得有关数据如表:下列说法正确的是( )
| 容 器 | 甲 | 乙 |
| 反应物投入量 | 2mol SO 2、1mol O 2 | 4mol SO 3 |
| n (SO 3)/mol | 1.6 | a |
| 反应物的转化率 | α 1 | α 2 |
| A. | α 1+α 2>1 | |
| B. | 1.6<a<3.2 | |
| C. | 若甲中反应2 min时达到平衡,则2 min 内平均速率 ν (O 2)=“0.2“molL -1min -1 | |
| D. | 甲平衡后再加入0.2 mol SO 2、0.2 mol O 2和0.4 mol SO 3,平衡逆向移动 |
4.0.1mol/LNa2S溶液,下列说法正确的是( )
| A. | c(Na+)=2c(S2-) | B. | c(OH-)=c(H+)+c(HS-)+2c(H2S) | ||
| C. | c(Na+)>c(S2-)>c(HS-)>c(OH-) | D. | c(Na+)+c(H+)=c(OH-)+c(HS-)+c(S2-) |
14.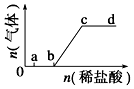 向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示.则下列离子组在对应的溶液中,一定能大量共存的是( )
向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示.则下列离子组在对应的溶液中,一定能大量共存的是( )
 向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示.则下列离子组在对应的溶液中,一定能大量共存的是( )
向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示.则下列离子组在对应的溶液中,一定能大量共存的是( )| A. | a点对应的溶液中:Na+、OH-、SO42-、NO3- | |
| B. | c点对应的溶液中:Na+、Ca2+、NO3-、Cl- | |
| C. | b点对应的溶液中:Al3+、Fe3+、NO3-、Cl- | |
| D. | d点对应的溶液中:Fe2+、Na+、Cl-、NO3- |
18.在一定的温度下,向饱和的烧碱溶液中放入一定量的过氧化钠,充分反应后恢复到原来的温度,下列说法正确的是( )
| A. | 溶液中Na+浓度增大,有O2放出 | B. | 溶液中OH-总数不变,有O2放出 | ||
| C. | 溶液的pH增大,有O2放出 | D. | 溶液中Na+总数减少,有O2放出 |
19.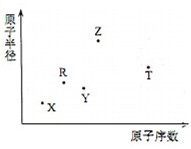 短周期主族元素X、Y、Z、R、T的原子半径与原子序数关系如图所示.R原子最外层电子数是电子层数的2倍.Y与Z能形成Z2Y、Z2Y2型离子化合物.Z与T形成的化合物Z2T.下列推断错误的是( )
短周期主族元素X、Y、Z、R、T的原子半径与原子序数关系如图所示.R原子最外层电子数是电子层数的2倍.Y与Z能形成Z2Y、Z2Y2型离子化合物.Z与T形成的化合物Z2T.下列推断错误的是( )
 短周期主族元素X、Y、Z、R、T的原子半径与原子序数关系如图所示.R原子最外层电子数是电子层数的2倍.Y与Z能形成Z2Y、Z2Y2型离子化合物.Z与T形成的化合物Z2T.下列推断错误的是( )
短周期主族元素X、Y、Z、R、T的原子半径与原子序数关系如图所示.R原子最外层电子数是电子层数的2倍.Y与Z能形成Z2Y、Z2Y2型离子化合物.Z与T形成的化合物Z2T.下列推断错误的是( )| A. | 形成的简单离子半径的大小顺序为T>Y>Z | |
| B. | Z2Y、Z2Y2所含有的化学键类型相同 | |
| C. | 0.005mol•L-1T的最高价氧化物对应水化物的水溶液pH等于2 | |
| D. | Z2T的水溶液显碱性,对水的电离有促进作用 |