��Ŀ����
���з�Ӧ��CO��g��+H2O��g��?CO2��g��+H2��g������H��0 ��850��ʱ��K=1��
��1�����¶Ƚ��͵�750��ʱ���ﵽƽ��ʱK 1������ڡ���С�ڡ����ڡ�����
��2��850��ʱ������һ�ݻ��ɱ���ܱ�������ͬʱ����1mol CO��3mol H2O��1mol CO2��x mol H2����
�ٵ�x=5.0ʱ������ƽ���� �������Ӧ�����淴Ӧ���������ƶ���
����Ҫʹ������Ӧ��ʼʱ������Ӧ������У���xӦ����������� ��
��3����850��ʱ������x=5.0��������Ӧ�ﵽƽ����H2����������ֱ�Ϊa%��a= ��
��1�����¶Ƚ��͵�750��ʱ���ﵽƽ��ʱK
��2��850��ʱ������һ�ݻ��ɱ���ܱ�������ͬʱ����1mol CO��3mol H2O��1mol CO2��x mol H2����
�ٵ�x=5.0ʱ������ƽ����
����Ҫʹ������Ӧ��ʼʱ������Ӧ������У���xӦ�����������
��3����850��ʱ������x=5.0��������Ӧ�ﵽƽ����H2����������ֱ�Ϊa%��a=
���㣺��ѧƽ���Ӱ������,��ѧƽ��ļ���
ר�⣺��ѧƽ��ר��
��������1����Ӧ�Ƿ��ȷ�Ӧ�������¶ȣ�ƽ��������У�
��2���ٷ�Ӧ���������ʵ���ϵ����ͬ��Ϊ1���������ʵ�������Ũ�ȣ�����Ũ����Qc������Ũ����Qc��ƽ�ⳣ��k�Ĺ�ϵ�жϣ�Qc��kƽ�����淴Ӧ���У�Qc=k��Ӧ����ƽ��״̬��Qc��kƽ��������Ӧ���У�
����x��ʾ��Ũ����Qc��ƽ��������Ӧ�ƶ���Ӧ����Ũ����Qc��k���ݴ˼����жϣ�
��3������ƽ�ⳣ��������ƽ���ƶ�����������㣮
��2���ٷ�Ӧ���������ʵ���ϵ����ͬ��Ϊ1���������ʵ�������Ũ�ȣ�����Ũ����Qc������Ũ����Qc��ƽ�ⳣ��k�Ĺ�ϵ�жϣ�Qc��kƽ�����淴Ӧ���У�Qc=k��Ӧ����ƽ��״̬��Qc��kƽ��������Ӧ���У�
����x��ʾ��Ũ����Qc��ƽ��������Ӧ�ƶ���Ӧ����Ũ����Qc��k���ݴ˼����жϣ�
��3������ƽ�ⳣ��������ƽ���ƶ�����������㣮
���
�⣺��1����Ӧ��CO��g��+H2O��g��?CO2��g��+H2��g����H��0��������ƽ��������У�ƽ�ⳣ��������1���ʴ�Ϊ�����ڣ�
��2���ٴ�ʱ��Ũ����Qc=
=1.67������ƽ�ⳣ��1����ƽ�����淴Ӧ�����ƶ����ʴ�Ϊ���淴Ӧ��
��ƽ��������Ӧ�����ƶ���Ũ����С��ƽ�ⳣ������
��1�����x��3.0���ʴ�Ϊ��x��3.0��
����850��ʱ������x=5.0����ʱŨ����Q=
=1.67������ƽ�ⳣ��1����ƽ�����淴Ӧ�����ƶ�����������Ӧ�ﵽƽ����������������ʵ���Ϊm
CO��g��+H2O��g��?CO2��g��+H2��g��
��ʼ����mol�� 1 3 1 5
�仯����mol�� m m m m
ƽ������mol�� 1+m 3+m 1-m 5-m
K=
=1
m=0.2mol
��H2����������ֱ�Ϊa%=
��100%=48%
�ʴ�Ϊ��48��
��2���ٴ�ʱ��Ũ����Qc=
| 1��5 |
| 1��3 |
��ƽ��������Ӧ�����ƶ���Ũ����С��ƽ�ⳣ������
| 1��x |
| 1��3 |
����850��ʱ������x=5.0����ʱŨ����Q=
| 1��5 |
| 1��3 |
CO��g��+H2O��g��?CO2��g��+H2��g��
��ʼ����mol�� 1 3 1 5
�仯����mol�� m m m m
ƽ������mol�� 1+m 3+m 1-m 5-m
K=
| (1-m)(5-m) |
| (1+m)(3+m) |
m=0.2mol
��H2����������ֱ�Ϊa%=
| (5-0.2)mol |
| (1+3+1+5)mol |
�ʴ�Ϊ��48��
���������⿼��ת���ʡ���ѧƽ���йؼ��㡢��ѧƽ���ƶ���Ӱ�����صȣ�ע��ƽ�ⳣ����Ӧ�á�ƽ���ƶ��ı����ǽ��Ĺؼ�����Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
 ��������ϵ�д�
��������ϵ�д� ���ɶ���ܲ��¿�ֱͨ�߿�ϵ�д�
���ɶ���ܲ��¿�ֱͨ�߿�ϵ�д�
�����Ŀ
����˵���У���ȷ���ǣ�������
A�� -OH�� -OH��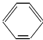 -CH2OH��Ϊͬϵ�� -CH2OH��Ϊͬϵ�� |
| B���Ҵ������ѻ�Ϊͬ���칹�� |
| C���Ҵ����Ҷ�������������Ϊͬϵ�� |
| D������Ũ��ˮ�������Ҵ����� |
����ʵ������ѡ�õ������������ǣ�������
| A����200mL��Ͳ��ȡ5.2mLϡ���� |
| B����250mL����ƿ����250mL0.2mol/L������������Һ |
| C����������ƽ����11.75g�Ȼ��ƾ��� |
| D���ü�ʽ�ζ�����ȡ25.10mL��ˮ |
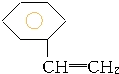 �� 4���л���ֱ���һ����������H2��ַ�Ӧ��
�� 4���л���ֱ���һ����������H2��ַ�Ӧ�� ���������ʣ�
���������ʣ� ��1������ͼװ�ý��й��ˣ�����a�����ƣ�
��1������ͼװ�ý��й��ˣ�����a�����ƣ�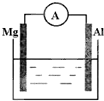 ��ͼ��ʾ�����һ��ԭ��أ�
��ͼ��ʾ�����һ��ԭ��أ�