题目内容
下表是元素周期表的一部分,回答下列有关问题:
(1)写出下列元素符号:① ,⑥ ,⑦ .
(2)画出原子的结构示意图:④ ,⑤ ,⑧ .
(3)在这些元素中,最活泼的金属元素是 ,最活泼的非金属元素是 ,最不活泼的元素是 .(均用元素符号表示)
(4)在这些元素的最高价氧化物对应水化物中,酸性最强的是 ,碱性最强的是 ,呈两性的氢氧化物是 .(均写出物质的化学式)
(1)写出下列元素符号:①
(2)画出原子的结构示意图:④
(3)在这些元素中,最活泼的金属元素是
(4)在这些元素的最高价氧化物对应水化物中,酸性最强的是
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅥⅠA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑾ | ⑿ |
考点:元素周期律和元素周期表的综合应用
专题:
分析:(1)根据元素在周期表中位置,可知①为N、②为F、③为Na、④为Mg、⑤为Al、⑥为Si、⑦为S、⑧为Cl、⑨为Ar、⑩为K、?为Ca、?为Br;
(2)④为Mg,原子核外有3个电子层,各层电子数为2、8、2;⑤为Al,原子核外有3个电子层,各层电子数为2、8、3;⑦为S,原子核外有3个电子层,各层电子数为2、8、6;
(3)同周期自左而右金属性减弱、非金属性增强,同主族自上而下金属性增强、非金属性减弱,稀有气体的化学性质最不活泼;
(4)高氯酸的酸性最强;K的金属性最强,故KOH的碱性最强;氢氧化铝是两性氢氧化物.
(2)④为Mg,原子核外有3个电子层,各层电子数为2、8、2;⑤为Al,原子核外有3个电子层,各层电子数为2、8、3;⑦为S,原子核外有3个电子层,各层电子数为2、8、6;
(3)同周期自左而右金属性减弱、非金属性增强,同主族自上而下金属性增强、非金属性减弱,稀有气体的化学性质最不活泼;
(4)高氯酸的酸性最强;K的金属性最强,故KOH的碱性最强;氢氧化铝是两性氢氧化物.
解答:
解:(1)根据元素在周期表中位置,可知①为N、②为F、③为Na、④为Mg、⑤为Al、⑥为Si、⑦为S、⑧为Cl、⑨为Ar、⑩为K、?为Ca、?为Br,
故答案为:N;Si;S;
(2)④为Mg,原子核外有3个电子层,各层电子数为2、8、2,原子结构示意图为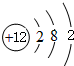 ;
;
⑤为Al,原子核外有3个电子层,各层电子数为2、8、3,原子结构示意图为 ;
;
⑦为S,原子核外有3个电子层,各层电子数为2、8、6,原子结构示意图为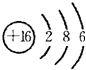 ,
,
故答案为: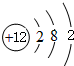 ;
; ;
; ;
;
(3)同周期自左而右金属性减弱、非金属性增强,同主族自上而下金属性增强、非金属性减弱,上述元素中,金属性最强的元素是K,非金属性最强的元素是F,稀有气体Ar的化学性质最不活泼,
故答案为:K;F;Ar;
(4)酸性最强是高氯酸,化学式为HClO4;K的金属性最强,故KOH的碱性最强;Al(OH)3是两性氢氧化物,故答案为:HClO4;KOH;Al(OH)3.
故答案为:N;Si;S;
(2)④为Mg,原子核外有3个电子层,各层电子数为2、8、2,原子结构示意图为
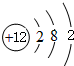 ;
;⑤为Al,原子核外有3个电子层,各层电子数为2、8、3,原子结构示意图为
 ;
;⑦为S,原子核外有3个电子层,各层电子数为2、8、6,原子结构示意图为
 ,
,故答案为:
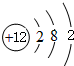 ;
; ;
; ;
;(3)同周期自左而右金属性减弱、非金属性增强,同主族自上而下金属性增强、非金属性减弱,上述元素中,金属性最强的元素是K,非金属性最强的元素是F,稀有气体Ar的化学性质最不活泼,
故答案为:K;F;Ar;
(4)酸性最强是高氯酸,化学式为HClO4;K的金属性最强,故KOH的碱性最强;Al(OH)3是两性氢氧化物,故答案为:HClO4;KOH;Al(OH)3.
点评:本题考查元素周期表与元素周期律,比较基础,注意对元素周期律的理解掌握,熟练掌握元素周期表的结构,有利于基础知识的巩固.

练习册系列答案
相关题目
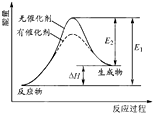 某反应的反应过程中能量的变化如图所示,图中E1表示正反应的活化能,E2表示逆反应的活化能,下列有关叙述正确的是( )
某反应的反应过程中能量的变化如图所示,图中E1表示正反应的活化能,E2表示逆反应的活化能,下列有关叙述正确的是( )| A、该反应为放热反应 |
| B、催化剂能改变该反应的焓变 |
| C、E1也可表示反应物断键需要吸收的总能量 |
| D、△H=E2-E1 |
下列各组性质的比较中不正确的是( )
| A、酸性 HClO4>HBrO4>HIO4 |
| B、碱性 Ba(OH)2>Ca(OH)2>Mg(OH)2 |
| C、稳定性 HCl>H2S>PH3 |
| D、氧化性 I>Br>Cl |
一定条件下,可逆反应N2+3H2?2NH3(正反应为放热反应)达到平衡,当单独改变下述条件后,有关叙述错误的是( )
| A、加催化剂,V正、V逆 都发生变化,且变化的倍数相等 |
| B、加压,V正、V逆 都增大,且V正 增大的倍数大于V逆增大的倍数 |
| C、降温,V正、V逆 都减小,且V正 减小的倍数大于V逆减小的倍数 |
| D、增大氮气的浓度,V正、V逆 都增大,且V正 增大倍数大于V逆 增大倍数;N2 转换率减小,H2转化率增大 |
在稀硫酸中加入铜粉,铜粉不溶解,再加入下列物质①FeCl3②Fe2O3③KNO3④H2O2铜粉能溶解的是( )
| A、只有①、② |
| B、只有①、②、④ |
| C、只有①、③、④ |
| D、上述任一一种 |