题目内容
4.已知1~18号元素的离子aW3+、bX+、cY2-、dZ-都具有相同的电子层结构,下列关系正确的是( )| A. | 质子数:c>b | B. | 离子半径:X+>Z- | C. | 稳定性:H2Y>HZ | D. | 碱性:XOH>W(OH)3 |
分析 1~18号元素的离子aW3+、bX+、cY2-、dZ-具有相同电子层结构,核外电子数相等,所以a-3=b-1=c+2=d+1,Y、Z为非金属,处于第二周期,故Y为O元素,Z为F元素,W、X为金属处于第三周期,W为Al元素,X为Na元素,结合元素周期律解答.
解答 解:元素周期表前三周期元素的离子aW3+、bX+、cY2-、dZ-具有相同电子层结构,核外电子数相等,所以a-3=b-1=c+2=d+1,Y、Z为非金属,应处于第二周期,故Y为O元素,Z为F元素,W、X为金属应处于第三周期,W为Al元素,X为Na元素,
A.离子的电子层结构相同,则b-1=c+2,则质子数b>c,故A错误;
B.电子层相同,核电荷数越多半径越小,所以离子半径:X+<Z-,故B错误;
C.非金属性越强,其氢化物的稳定性越强,非金属性Y<Z,则氢化物的稳定性H2Y<HZ,故C错误;
D.W是Al元素、X是Na元素,金属性越强最高价氧化物对应水化物的碱性越强,所以碱性:XOH>W(OH)3,故D正确;
故选D.
点评 本题考查原子结构和元素性质,为高频考点,正确判断元素是解本题关键,熟练掌握同一周期、同一主族元素原子结构、元素性质递变规律,题目难度不大.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案
相关题目
15.近年来,科学家研制出一种新型的乙醇电池,它用酸性电解质(H+)作溶剂.电池总反应为 C2H5OH+3O2═2CO2+3H2O,下列说法不正确的是( )
| A. | 乙醇在电池的负极上参加反应 | |
| B. | 1 mol C2H5OH被氧化时,有6 mol电子转移 | |
| C. | 随着反应的进行,正极附近溶液的酸性减弱 | |
| D. | 电池的正极反应为2H2O+O2+4e- 4OH- |
19.下列粒子的结构示意图中,表示氟离子的是( )
| A. | 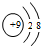 | B. | 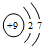 | C. | 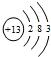 | D. | 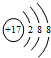 |
9.一定温度下,对反应2A(g)+B(s)?2C(g)能说明其达到平衡状态的是( )
| A. | 容积中A、B、C三者共存 | |
| B. | 单位时间内反应的A与生成的C的物质的量之比为1:1 | |
| C. | c(A):c(B):c(C)=2:1:2 | |
| D. | 气体的总质量不再发生变化 |
16.在下列化学反应中,既有离子键、共价键断裂,又有离子键、共价键形成的是( )
| A. | 2Na+2H2O═2NaOH+H2↑ | B. | SO2+2H2S═3S↓+2H2O | ||
| C. | Mg3N2+6H2O═3Mg(OH)2↓+2NH3↑ | D. | AgNO3+NaCl═AgCl↓+NaNO3 |
13.分子式为CnH2n+1X(n≠1)的卤代烃不能发生消去反应,n的最小值是( )
| A. | 2 | B. | 3 | C. | 4 | D. | 5 |
 ;
;
 .
.