题目内容
VA族元素包括氮(N)、磷(P)、砷(As)、锑(Sb)、铋(Bi)等元素,含VA族元素的化合物在科研和生产中有许多重要用途.请回答下列问题:
(1)原子的第一电离能是指气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量,N、P、As原子的第一电离能由大到小的顺序为 ,
(2)As的原子序数为 ,其核外价电子排布图为 .
(3)NH3的稳定性比PH3的稳定性 (填“强”或“弱”),PCl3分子中P的杂化方式为 ,PO43-的立体构型为 .
(4)无机含氧酸分子中非羟基氧数目越多酸性越强,根据这一规律判断H3PO4的酸性比HNO3 (填“强”或“弱”),原因是
(5)NH3极易溶于水是因为有氢键作用,请画出氨气的水溶液中可能存在的氢键 .
(1)原子的第一电离能是指气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量,N、P、As原子的第一电离能由大到小的顺序为
(2)As的原子序数为
(3)NH3的稳定性比PH3的稳定性
(4)无机含氧酸分子中非羟基氧数目越多酸性越强,根据这一规律判断H3PO4的酸性比HNO3
(5)NH3极易溶于水是因为有氢键作用,请画出氨气的水溶液中可能存在的氢键
考点:元素电离能、电负性的含义及应用,原子核外电子排布,原子轨道杂化方式及杂化类型判断,含有氢键的物质
专题:原子组成与结构专题,化学键与晶体结构
分析:(1)元素的非金属性越强,其得电子能力越强,失电子能力越弱,则第一电离能越大;
(2)As原子序数为33,M层上有18个电子,N层上有5个电子;
(3)非金属性越强,对应氢化物越稳定;根据价层电子对互斥理论确定分子或离子中中心原子的价层电子对数,再判断杂化类型和空间构型;
(4)根据含氧酸都可写成(HO)m ROn形式,n值越大,酸性越强来解答;
(5)N元素与O元素的电负性都很强,不同分子中的N原子、O原子与H原子之间都可以形成氢键.
(2)As原子序数为33,M层上有18个电子,N层上有5个电子;
(3)非金属性越强,对应氢化物越稳定;根据价层电子对互斥理论确定分子或离子中中心原子的价层电子对数,再判断杂化类型和空间构型;
(4)根据含氧酸都可写成(HO)m ROn形式,n值越大,酸性越强来解答;
(5)N元素与O元素的电负性都很强,不同分子中的N原子、O原子与H原子之间都可以形成氢键.
解答:
解:(1)同一主族元素中,元素的金属性随着原子序数的增大而增强,失电子能力增强,也就是越容易失电子,电离能越小,则第一电离能随着原子序数的增大而减小,所以这几种元素第一电离能大小顺序是N>P>As,
故答案为:N>P>As;
(2)As原子序数为33,最外层有5个电子,根据构造原理知,其价电子的电子排布式为4s24p3,则核外价电子排布图为: ;
;
故答案为:33; ;
;
(3)非金属性越强,对应氢化物越稳定,非金属性:N>P,则NH3的稳定性比PH3的稳定性强;PCl3分子中P的价层电子对数=3+
(5-3×1)=4,属于sp3杂化;PO43-中心原子为P,其中σ键电子对数为4,中心原子孤电子对数为
(5+3-4×2)=0,PO43-价层电子对对数为4+0=4,故PO43-的立体构型为正四面体;
故答案为:强;sp3;正四面体;
(4)含氧酸的强度随着分子中连接在中心原子上的非羟基氧的个数增大而增大,H3PO4可写成(HO)3PO,n=1,HNO2可写成(HO)NO2,n=2,所以H3PO4的酸性比HNO3弱,
故答案为:弱;含氧酸的强度随着分子中连接在中心原子上的非羟基氧的个数增多而增大,H3PO4 中含有一个非羟基氧原子,HNO3 中含有两个非羟基氧原子;
(5)N元素与O元素的电负性都很强,不同分子中的N原子、O原子与H原子之间都可以形成氢键,如O-H…N、N-H…O、O-H…O、N-H…N,
故答案为:O-H…N;N-H…O;O-H…O;N-H…N.
故答案为:N>P>As;
(2)As原子序数为33,最外层有5个电子,根据构造原理知,其价电子的电子排布式为4s24p3,则核外价电子排布图为:
 ;
;故答案为:33;
 ;
;(3)非金属性越强,对应氢化物越稳定,非金属性:N>P,则NH3的稳定性比PH3的稳定性强;PCl3分子中P的价层电子对数=3+
| 1 |
| 2 |
| 1 |
| 2 |
故答案为:强;sp3;正四面体;
(4)含氧酸的强度随着分子中连接在中心原子上的非羟基氧的个数增大而增大,H3PO4可写成(HO)3PO,n=1,HNO2可写成(HO)NO2,n=2,所以H3PO4的酸性比HNO3弱,
故答案为:弱;含氧酸的强度随着分子中连接在中心原子上的非羟基氧的个数增多而增大,H3PO4 中含有一个非羟基氧原子,HNO3 中含有两个非羟基氧原子;
(5)N元素与O元素的电负性都很强,不同分子中的N原子、O原子与H原子之间都可以形成氢键,如O-H…N、N-H…O、O-H…O、N-H…N,
故答案为:O-H…N;N-H…O;O-H…O;N-H…N.
点评:本题考查物质结构和性质,涉及电负性、杂化方式的判断、电子排布式的书写、氢键等,侧重于基础知识的综合应用的考查,题目难度中等,注意书写电子排布式时要符合构造原理,为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列元素的第一电离能依次减小的是( )
| A、H、Li、Na、K |
| B、I、Br、Cl、F |
| C、Na、Mg、Al、Si |
| D、Si、Al、Mg、Na |
经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键.下列判断正确的是( )
| A、AlCl3为离子化合物 |
| B、P 与Cl可形成共价键 |
| C、SiCl4为共价化合物 |
| D、K与Mg 形成共价键 |
某组成为C5H12O的醇可被氧化成为C5H10O2的酸,具有这种结构的醇的同分异构体共有( )
| A、2种 | B、4种 | C、8种 | D、14种 |
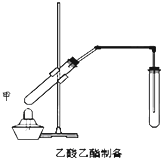 如图在试管甲中先加入2mL 95%的乙醇,并在摇动下缓缓加入2mL浓硫酸,充分摇匀,冷却后再加入2克无水乙酸钠,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管乙中加入5ml 饱和的碳酸钠溶液,按图连接好装置,用酒精灯对试管甲小火加热3~5min后,改用大火加热,当观察到左试管中有明显现象时停止实验.试回答:
如图在试管甲中先加入2mL 95%的乙醇,并在摇动下缓缓加入2mL浓硫酸,充分摇匀,冷却后再加入2克无水乙酸钠,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管乙中加入5ml 饱和的碳酸钠溶液,按图连接好装置,用酒精灯对试管甲小火加热3~5min后,改用大火加热,当观察到左试管中有明显现象时停止实验.试回答: 在实验室,可以用如图所示的装置制取乙酸乙酯.回答下列问题:
在实验室,可以用如图所示的装置制取乙酸乙酯.回答下列问题: