��Ŀ����
��12�֣�2013���������������Ű�ҹ��ж������������У�����β����ȼúβ������ɿ�����Ⱦ��ԭ��֮һ��
��1��CO2�Ǵ����к�����ߵ�һ���������壬���ƺ�����CO2�ǽ������ЧӦ����Ч;����Ŀǰ����CO2���ϳɶ�������ȡ���˽ϴ�Ľ�չ���仯ѧ��Ӧ�ǣ�
2CO2��g��+6H2��g�� CH3OCH3��g��+3H2O��g�� ��H��0��
CH3OCH3��g��+3H2O��g�� ��H��0��
��д���÷�Ӧ��ƽ�ⳣ������ʽ ��
���жϸ÷�Ӧ��һ�������£�����㶨���ܱ��������Ƿ�ﵽ��ѧƽ��״̬�������� ��
A���������ܶȲ���
B����λʱ��������2molCO2��ͬʱ����1mol������
C��v(CO2)�Uv(H2)=1�U3
D��������ѹǿ���ֲ���
��2������β����������Ҫԭ��Ϊ��2NO(g)+2CO (g)  2CO2 (g) +N2 (g) ���ܱ������з����÷�Ӧʱ��c(CO2)���¶�(T)�������ı����(S)��ʱ��(t)�ı仯���ߣ���ͼ��ʾ��
2CO2 (g) +N2 (g) ���ܱ������з����÷�Ӧʱ��c(CO2)���¶�(T)�������ı����(S)��ʱ��(t)�ı仯���ߣ���ͼ��ʾ��

�ݴ��жϣ�
�ٸ÷�Ӧ�Ħ�H 0��ѡ�����������������
�ڵ��������������һ��ʱ�����������������ѧ��Ӧ���ʡ��������ı����S1��S2������ͼ�л���c(CO2)��T2��S2�����´ﵽƽ������еı仯���ߡ�
��3����֪��CO��g���� 2H2��g�� CH3OH��g����H = -a kJ?mol-1��
CH3OH��g����H = -a kJ?mol-1��
�پ��ⶨ��ͬ�¶��¸÷�Ӧ��ƽ�ⳣ�����£�
�¶ȣ��棩 | 250 | 300 | 350 |
K | 2.041 | 0.270 | 0.012 |
��ijʱ�̡�250���ø÷�Ӧ�ķ�Ӧ�����������Ũ��Ϊc(CO)=0.4 mol��L��1��c(H2)=0.4 mol��L��1��c(CH3OH)=0.8 mol��L��1, ���ʱv�� v�棨���������������=������
��ij�¶��£�������̶���2L���ܱ������н�1 mol CO��2 mol H2��ϣ���ò�ͬʱ�̵ķ�Ӧǰ��ѹǿ��ϵ���£�
ʱ�䣨min�� | 5 | 10 | 15 | 20 | 25 | 30 |
ѹǿ��(P��/Pǰ) | 0.98 | 0.90 | 0.80 | 0.70 | 0.70 | 0.70 |
�ﵽƽ��ʱCO��ת����Ϊ ��
��1���� ��B��D��2�֣���ѡ1����1�֣�
��2���٣�
�ڣ�2�֣�

��3���٣���2�֣� �� 45%��2�֣�
��������
�����������1���ٸ����������ʽд���÷�Ӧ��ƽ�ⳣ������ʽ
K=c��CH3OCH3����c3��H2O��/c2��CO2��c6��H2������A����������㶨��������������䣬�ܶȲ��淴Ӧ�Ľ��ж��仯���ܶȲ��䲻����Ϊƽ���־������B����λʱ��������2molCO2��ͬʱ����1mol�����ѣ������淴Ӧ������ȣ�����ƽ���־����ȷ��C��û����ȷ�����淴Ӧ���ʣ�v(CO2)�Uv(H2)=1�U3 ������Ϊƽ���־������D���÷�ӦΪ��Ӧǰ���������ʵ������ȵķ�Ӧ��������ѹǿ�淴Ӧ�Ľ��в��ϱ仯��������ѹǿ���ֲ����Ѵ�ƽ��״̬����ȷ��ѡBD����2���� ��ͼ���֪�¶�ΪT1ʱ��Ӧ�ȴﵽƽ�⣬��Ӧ���ʿ죬���¶ȣ�T1��T2,�¶�ΪT1ʱ������̼��ƽ��Ũ��С��˵�������¶�ƽ�������ƶ�������ӦΪ���ȷ�Ӧ����H��0���ڸ��������Ϣ֪���������������һ��ʱ�����������������ѧ��Ӧ���ʣ����̴�ƽ���ʱ�䣬��ƽ�ⲻ�ƶ���������̼��ƽ��Ũ�Ȳ��䣬ͼ����𰸣�(3���ٸ����������ʽ�����ݼ���Q= c��CH3OH��/c2��H2��c��CO��=0.8/0.4��0.42=12.5���ɱ�������֪250��ʱK=2.041��Q��K����Ӧ������У���ʱv����v�棻�ڸ�������ʽ���㣬��ת����CO�����ʵ���Ϊx��
CO��g���� 2H2��g��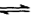 CH3OH��g��
CH3OH��g��
��ʼ����mol��1 2 0
ת������mol��x 2x x
ƽ������mol��1��x 2��2 x x
���ݱ�������֪��ƽ���P��/Pǰ=0.70�����ݰ����ӵ����ɣ����µ���ʱѹǿ֮�ȵ�����������ʵ���֮�ȼ�(3��2x)/3=0.70�����x=0.45��һ����̼��ת����Ϊ45%��
���㣺���黯ѧ��Ӧ���ʺͻ�ѧƽ�⡣


 �����Ա�ʾ12C��Ҳ���Ա�ʾ14C
�����Ա�ʾ12C��Ҳ���Ա�ʾ14C �����Ա�ʾ������̼���ӣ�Ҳ���Ա�ʾˮ����
�����Ա�ʾ������̼���ӣ�Ҳ���Ա�ʾˮ���� ���Ա�ʾ�ǻ���Ҳ���Ա�ʾ����������
���Ա�ʾ�ǻ���Ҳ���Ա�ʾ����������
 CO(g)��3H2(g) ��H����206.4 kJ��mol��1
CO(g)��3H2(g) ��H����206.4 kJ��mol��1 ��100%������������С�����1λ��
��100%������������С�����1λ��
 2Z(g),��X��Y��Z����ʼŨ�ȷֱ�Ϊc1��c2��c3 ������Ϊ�㣩����Ӧ�ﵽƽ��ʱ,X��Y��Z��Ũ�ȷֱ�Ϊ0.1mol?L-1��0.3 mol?L-1��0.08 mol?L-1.�������жϲ���ȷ����
2Z(g),��X��Y��Z����ʼŨ�ȷֱ�Ϊc1��c2��c3 ������Ϊ�㣩����Ӧ�ﵽƽ��ʱ,X��Y��Z��Ũ�ȷֱ�Ϊ0.1mol?L-1��0.3 mol?L-1��0.08 mol?L-1.�������жϲ���ȷ����

 PbCl42�� (aq) ��H��0
PbCl42�� (aq) ��H��0