题目内容
(8分)实验室要用98%(ρ="1.84" g·cm-3)的硫酸配制3.68 mol·L-1的硫酸溶液400mL
(1)计算所需98%的硫酸 mL
(2)该实验中除了要用到量筒、烧杯以外,还需要用到的玻璃仪器(无需装瓶)有: 、 、 。
(3)若配制3.68mol·L-1的硫酸溶液的其他操作均正确,但出现下列错误操作,将导致所配制的硫酸溶液浓度偏低的是 。
| A.浓硫酸溶解后未冷却,直接转移至容量瓶后定容 |
| B.将烧杯内的稀硫酸向容量瓶中转移时,因操作不当使部分稀硫酸溅出瓶外 |
| C.用量筒量取浓硫酸时,俯视读数 |
| D.容量瓶使用前用3.68mol·L-1硫酸的溶液润洗 |
(1)100
(2)玻璃棒、胶头滴管、500ml容量瓶
(3)BC
解析试题分析:(1)98%(ρ="1.84" g·cm-3)的硫酸的物质的量浓度是1000mL/L×1.84 g·cm-3×98%/98g/mol=18.4mol/L,根据容量瓶的规格,应配制500mL3.68 mol·L-1的硫酸溶液,根据配制溶液过程中,溶质的物质的量不变,所以需要浓硫酸的体积V=0.5L×3.68mol/L/18.4mol/L=0.1L=100mL;
(2)该实验中除了要用到量筒、烧杯以外,还需要用到的玻璃仪器有500mL的容量瓶盛放溶液,玻璃棒转移溶液,胶头滴管用于定容;
(3)A、浓硫酸溶解后未冷却,直接转移至容量瓶后定容,则冷却后溶液的体积偏少,所以所配溶液的浓度偏高,错误;B、将烧杯内的稀硫酸向容量瓶中转移时,因操作不当使部分稀硫酸溅出瓶外,使硫酸的物质的量减少,所以溶液的浓度偏低,正确;C、用量筒量取浓硫酸时,俯视读数,使量取的浓硫酸的体积偏少,所以硫酸的物质的量偏少,所配稀硫酸的物质的量浓度偏低,正确;D、容量瓶使用前用3.68mol·L-1硫酸的溶液润洗,则容量瓶内的硫酸物质的量增加,所以所配溶液的浓度偏高,错误,答案选BC。
考点:考查溶液的配制、计算与误差分析

 53随堂测系列答案
53随堂测系列答案上海环保部门为了使城市生活垃圾得到合理利用,近年来逐步实施了生活垃圾分类的方法。其中塑料袋、废纸、旧橡胶制品等属于
| A.无机物 | B.有机物 | C.盐类 | D.非金属单质 |
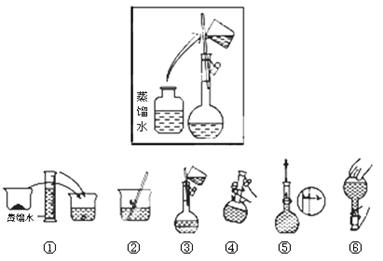
12分)现用质量分数为98%、密度为1.84 g·cm-3的浓H2SO4来配制500 mL 0.2 mol·L-1的稀H2SO4。可供选择的仪器有:①玻璃棒 ②烧瓶 ③烧杯 ④药匙 ⑤量筒 ⑥容量瓶 ⑦托盘天平。
请回答下列问题:
(1)上述仪器中,在配制稀H2SO4时用不到的有 (填代号)。配制时还欠缺的仪器是 。
(2)经计算,需浓H2SO4的体积为 mL(精确到0.1)。
(3)配制过程有以下操作:
| A.移液 |
| B.量取 |
| C.洗涤 |
| D.定容 |
F.摇匀
其正确的操作顺序应是 (填序号)。
(4)在配制过程中,其他操作都准确,下列操作中,能引起误差偏高的有 (填代号)。
①洗涤量取浓H2SO4后的量筒,并将洗涤液转移到容量瓶中
②稀释后的H2SO4溶液未等冷却至室温就转移到容量瓶中
③定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线
④转移前,容量瓶中含有少量蒸馏水
⑤定容时,俯视标线
(5)从上述容量瓶中移取25.00mL的稀硫酸溶液于100mL的容量瓶,加水稀释至刻度线。请问所得溶液中c(H+)= 。
(6)某研究小组欲利用氯气和二氧化硫通入水溶液中来制备100mL含0.4molH+的溶液,反应原理:Cl2+SO2+2H2O= H2SO4+2HCl,若忽略制备过程中气体的损耗,请问需标准状况下的氯气 L。
(10分)“84消毒液”能有效杀灭甲型H1N1病毒,某同学购买了一瓶“威露士”牌“84消毒液”,并查阅相关资料和消毒液包装说明得到如下信息:“84消毒液”:含25%NaClO、1 000 mL、密度1.192 g·cm-3,稀释100倍(体积比)后使用。
请根据以上信息和相关知识回答下列问题:
(1)该“84消毒液”的物质的量浓度为________mol·L-1。
(2)该同学取100 mL“威露士”牌“84消毒液”稀释后用于消毒,稀释后的溶液中
c(Na+)=________mol·L-1。
(3)一瓶“威露士”牌“84消毒液”能吸收空气中________L的CO2(标准状况)而变质。(已知:CO2+2NaClO+H2O===Na2CO3+2HClO)
(4)该同学参阅“威露士”牌“84消毒液”的配方,欲用NaClO固体配制480 mL含25%NaClO的消毒液。下列说法正确的是________。
| A.如上图所示的仪器中,有四种是不需要的,还需一种玻璃仪器 |
| B.容量瓶用蒸馏水洗净后,应烘干才能用于溶液配制 |
| C.利用购买的商品NaClO来配制可能导致结果偏低 |
| D.需要称量的NaClO固体质量为143 g |
向物质M的溶液中逐滴加入NaOH溶液,先产生白色沉淀,然后沉淀逐渐溶解,则物质M可能是
| A.MgSO4 | B.NaAlO2 | C.AlCl3 | D.FeCl3 |