题目内容
在一定条件下,Na2CO3溶液存在水解平衡:CO32-+H2O?HCO3-+OH-.下列说法正确的是( )
| A、稀释溶液,水解程度减小 | ||||||
| B、通入CO2,平衡朝正反应方向移动 | ||||||
C、升高温度,
| ||||||
| D、加入NaOH固体,溶液PH减小 |
考点:影响盐类水解程度的主要因素
专题:盐类的水解专题
分析:A.加水稀释,促进水解;
B、通入二氧化碳和氢氧根离子反应促进水解;
C、水解反应是吸热反应,升温促进水解;
D、碳酸根离子水解显碱性,加碱抑制水解.
B、通入二氧化碳和氢氧根离子反应促进水解;
C、水解反应是吸热反应,升温促进水解;
D、碳酸根离子水解显碱性,加碱抑制水解.
解答:
解:A.稀释溶液,促进水解,所以水解程度增大,故A错误;
B、CO2通入水中,生成H2CO3,可以与OH-反应,平衡正向移动,故B正确;
C、因水解是吸热的,则升温可以促进水解,平衡正向移动,
是增大的,故C错误;
D、加入NaOH固体,碱性肯定增强,pH增大,故D错误;
故选B.
B、CO2通入水中,生成H2CO3,可以与OH-反应,平衡正向移动,故B正确;
C、因水解是吸热的,则升温可以促进水解,平衡正向移动,
c(HC
| ||
c(C
|
D、加入NaOH固体,碱性肯定增强,pH增大,故D错误;
故选B.
点评:本题考查了水解平衡的影响因素,化学平衡移动原理同样适合水解平衡的移动,要多迁移,多联系.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案
相关题目
在配制一定物质的量浓度的NaOH溶液时,下列仪器肯定不需要的是( )
A、 |
B、 |
C、 |
D、 |
反应2A(g)?2B(g)+C(g)△H>0,要使逆反应速率增大,A的浓度减小(只改变一个条件),应采取的措施是( )
| A、减压 | B、升温 |
| C、加入合适的催化剂 | D、增大B的浓度 |
下列各种说法中,都包含有前后两个数值,其中前者大于后者的是( )
| A、在25℃和80℃时纯水中的c[H+]浓度 |
| B、室温时,浓度均为 0.1 mol?L-1的 (NH4)2SO4(aq)、(NH4)2CO3(aq)的 c (NH4+) |
| C、相同条件下,0.l mol?L-1 NaHCO3和 0.1 mol?L-1Na2CO3溶液的 pH |
| D、1 L饱和CH3COONa溶液中CH3COO-和Na+的个数 |
室温下向10mLpH=3的醋酸溶液中加入水稀释后,下列说法正确的是( )
| A、溶液中导电粒子的数目增加,导电性增强 | ||
| B、醋酸的电离程度增大,c(H+)亦增大 | ||
| C、再加入10mLpH=11NaOH溶液,混合液pH=7 | ||
D、溶液中
|
下列由极性键构成的非极性分子是( )
| A、N2 |
| B、HF |
| C、NH3 |
| D、CO2 |
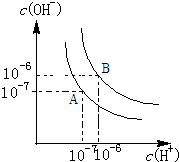 水的电离平衡如图所示.
水的电离平衡如图所示.