题目内容
5.化学知识在生产、生活、科技、环境等领域有着重要的应用,下列有关说法正确的是( )| A. | 门捷列夫利用软锰矿和浓盐酸反应制得了氯气 | |
| B. | 利用火力发电厂及核电站用于冷却的循环海水来提取单质溴以减少能耗 | |
| C. | 含重金属离子的污水的排放产生“赤潮”或“水华”等水污染现象 | |
| D. | 钢化玻璃、有机玻璃、防弹玻璃均属于硅酸盐材料 |
分析 A.瑞典化学家舍勒将软锰矿(主要成分是MnO2)与浓盐酸混合加热,在世界上首先制得了氯气;
B.火力发电厂及核电站用于冷却的循环海水含有较高热量;
C.根据水华、赤潮的形成原因;
D.普通玻璃的组成成分是Na2SiO3、CaSiO3、SiO2;
解答 解:A.瑞典化学家舍勒将软锰矿(主要成分是MnO2)与浓盐酸混合加热,在世界上首先制得了氯气,故A错误;
B.火力发电厂及核电站用于冷却的循环海水含有较高热量,用来提取单质溴以减少能耗,故B正确;
C.水华、赤潮是水体中某些微小的浮游植物、原生动物或细菌,在一定的环境条件下突发性地增殖和聚集,引起一定范围内一段时间中水体变色现象,含氮、磷的大量污水任意排放造成造成水体的富营养化,引发水华、赤潮.故C错误;
D.钢化玻璃既是将普通玻璃加热熔融后再急速冷却,故主要成分仍为硅酸盐;而有机玻璃的主要成分是有机物,不是硅酸盐,故D错误;
故选:B.
点评 本题考查了氯气的制备、海水提溴、水体的富营养化、常见硅酸盐材料,熟悉相关工艺流程,明确“赤潮”或“水华”等水污染现象原因是解题关键,题目难度不大.

练习册系列答案
相关题目
13.下列叙述中正确的是( )
| A. | 除零族元素外,短周期元素的最高化合价在数值上都等于该元素所属的族序数 | |
| B. | 除短周期外,其他周期均有18种元素 | |
| C. | 碱金属元素是指ⅠA族的所有元素 | |
| D. | 副族元素中没有非金属元素 |
10.下列各装置能够达到相应实验目的是( )
| A. |  用装置除去乙酸乙酯中混有的少量乙酸 | |
| B. |  用装置除去氯气中的少量氯化氢 | |
| C. | 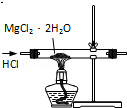 用装置制取无水MgCl2 | |
| D. |  用装置制取乙烯 |
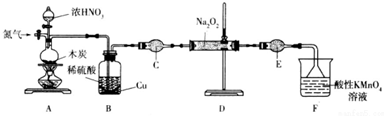

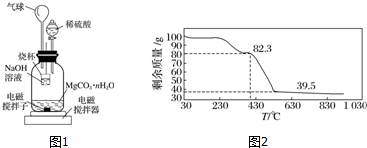
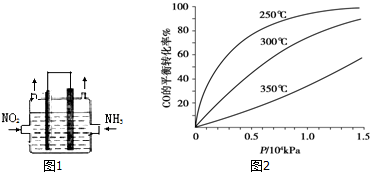
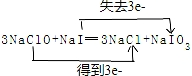 ,还原剂与氧化剂的物质的量之比是1:3.
,还原剂与氧化剂的物质的量之比是1:3.