题目内容
6.下列关于钠的化合物的说法中,正确的是( )| A. | Na2CO3和NaHCO3均能与盐酸和NaOH溶液反应 | |
| B. | Na2CO3固体中含有的NaHCO3可用加热的方法除去 | |
| C. | Na2O2和Na2O均为白色固体,与CO2反应均放出O2 | |
| D. | 分别向Na2CO3和NaHCO3与澄清石灰水反应,现象不相同 |
分析 A.Na2CO3与NaOH不反应;
B.NaHCO3加热分解生成碳酸钠;
C.Na2O2为淡黄色固体,氧化钠与二氧化碳反应生成碳酸钠;
D.Na2CO3和NaHCO3与澄清石灰水反应,均生成碳酸钙沉淀.
解答 解:A.Na2CO3与NaOH不反应,则NaHCO3能与盐酸和NaOH溶液反应,故A错误;
B.NaHCO3加热分解生成碳酸钠,则加热法可除杂,故B正确;
C.Na2O2为淡黄色固体,氧化钠与二氧化碳反应生成碳酸钠,过氧化钠与二氧化碳反应生成氧气,故C错误;
D.Na2CO3和NaHCO3与澄清石灰水反应,均生成碳酸钙沉淀,现象相同,故D错误;
故选B.
点评 本题考查钠的化合物的性质,为高频考点,把握溶物质的性质、发生的反应为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
相关题目
16.在标准状态下,二氧化碳气体的密度是( )
| A. | 1.964g/L | B. | 0.5091g/L | C. | 1.964g/mL | D. | 0.5091g/mL |
17.下列各组离子在无色酸性溶液中可以大量共存的有( )
| A. | Ag+、K+、NO3-、Cl - | B. | K+、Cu2+、SO42-、HCO3- | ||
| C. | Mg2+、Cl-、SO42-、Na+ | D. | CO32-、K+、NO3-、Na+ |
14.下列液体均处于25℃,有关叙述正确的是( )
| A. | 某物质的溶液pH<7,则该物质一定是酸 | |
| B. | 等物质的量浓度的Na2CO3溶液的碱性强于NaHCO3溶液 | |
| C. | pH=4的番茄汁中c(H+)是pH=6的牛奶中c(H+)的2倍 | |
| D. | AgCl在相同物质的量浓度的CaCl2和NaCl溶液中的溶解度相同 |
11.化学与生活密切相关,生活中的某些问题,常需用化学知识解释,下列说法不正确的是( )
| A. | 医疗中用75%的乙醇溶液进行消毒,是由于蛋白质遇酒精会变性 | |
| B. | 臭氧可用于自来水消毒,是因为臭氧具有强氧化性能杀死水中的病菌 | |
| C. | 腌制熟食品时,添加少量NaNO2,是为了使其味道更加美味可口 | |
| D. | 食盐中加入少量碘酸钾,食用后可补充人体内碘元素的不足 |
18.下列化学用语表示正确的是( )
| A. | 甲烷的结构式:CH4 | |
| B. | 硫离子的结构示意图: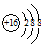 | |
| C. | Na2S的电子式: | |
| D. | 硫酸钠电离方程式:Na2SO4=Na2++SO42- |
16.下列有关叙述中正确的是( )
| A. | 在元素周期表金属与非金属的分界处可以寻找催化剂和耐高温、耐腐蚀的合金材料 | |
| B. | 两种微粒,若核外电子排布完全相同,则其化学性质一定相同 | |
| C. | 水分子很稳定,是因为水中存在氢键 | |
| D. | 在多电子的原子里,能量高的电子通常在离核远的区域内活动 |
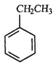 (g)+CO2(g)?
(g)+CO2(g)?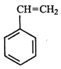 (g)=CO(g)+H2O(g)△H,其中乙苯在CO2气氛中的反应可分两步进行
(g)=CO(g)+H2O(g)△H,其中乙苯在CO2气氛中的反应可分两步进行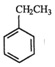 (g)?
(g)?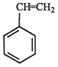 (g)+H2(g)△H1=-125KJ/mol
(g)+H2(g)△H1=-125KJ/mol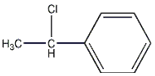 .
.