题目内容
a mol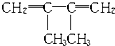 和b mol CH2=CH-CN按一定比例加聚成高分子化合物A.一定量的A完全燃烧生成CO2(g)、H2O(g)和N2(g),其中CO2的体积分数为57.14%,则形成A的两有机物的物质的量比为( )
和b mol CH2=CH-CN按一定比例加聚成高分子化合物A.一定量的A完全燃烧生成CO2(g)、H2O(g)和N2(g),其中CO2的体积分数为57.14%,则形成A的两有机物的物质的量比为( )
 和b mol CH2=CH-CN按一定比例加聚成高分子化合物A.一定量的A完全燃烧生成CO2(g)、H2O(g)和N2(g),其中CO2的体积分数为57.14%,则形成A的两有机物的物质的量比为( )
和b mol CH2=CH-CN按一定比例加聚成高分子化合物A.一定量的A完全燃烧生成CO2(g)、H2O(g)和N2(g),其中CO2的体积分数为57.14%,则形成A的两有机物的物质的量比为( )| A、1:1 | B、1:2 |
| C、2:3 | D、3:4 |
考点:化学方程式的有关计算
专题:计算题
分析:相同条件下,气体的物质的量之比等于其体积分数之比,根据原子守恒知,A完全反应生成的C原子个数等于两种有机物中碳原子个数,再根据碳原子的物质的量分数计算.
解答:
解:相同条件下,气体的物质的量之比等于其体积分数之比,二氧化碳的体积分数为57.14%,则二氧化碳物质的量分数为57.14%,
a mol 和b mol CH2=CH-CN按一定比例加聚成高分子化合物A,一定量的A完全燃烧生成CO2(g)、H2O(g)和N2(g),根据原子守恒知,生成二氧化碳的物质的量=(6a+3b)mol,水的物质的量=
和b mol CH2=CH-CN按一定比例加聚成高分子化合物A,一定量的A完全燃烧生成CO2(g)、H2O(g)和N2(g),根据原子守恒知,生成二氧化碳的物质的量=(6a+3b)mol,水的物质的量=
mol,氮气的物质的量=
mol,则二氧化碳的物质的量分数=
×100%=57.14%,则a:b=1:2,故选B.
a mol
 和b mol CH2=CH-CN按一定比例加聚成高分子化合物A,一定量的A完全燃烧生成CO2(g)、H2O(g)和N2(g),根据原子守恒知,生成二氧化碳的物质的量=(6a+3b)mol,水的物质的量=
和b mol CH2=CH-CN按一定比例加聚成高分子化合物A,一定量的A完全燃烧生成CO2(g)、H2O(g)和N2(g),根据原子守恒知,生成二氧化碳的物质的量=(6a+3b)mol,水的物质的量=| 10a+3b |
| 2 |
| b |
| 2 |
| 6a+3b |
| 6a+3b+5a+1.5b+0.5b |
点评:本题考查了物质的量的有关计算,明确体积分数等于其物质的量分数是解本题关键,再结合原子守恒进行解答,题目难度不大.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
已知NaHSO4在水中的电离方程式为:NaHSO4=Na++H++SO42-.某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2.下列对该溶液的叙述中,不正确的是( )
| A、该温度为常温25℃ |
| B、由水电离出来的H+的浓度是1.0×10-12mol?L-1 |
| C、加入NaHSO4晶体抑制了水的电离 |
| D、该温度下加入等体积浓度为0.01 mol/L的NaOH溶液可使该溶液恰好呈中性 |
下列反应的离子方程式书写正确的是( )
A、向NH4HCO3溶液中少量的NaOH溶液并加热:NH4++OH-
| ||||
| B、用稀HNO3溶解FeS固体:FeS+2H+═Fe2++H2S↑ | ||||
| C、向NaHCO3溶液中加过量澄清石灰水:2HCO3-+Ca2++2OH-═CaCO3↓+CO32-+2H2O | ||||
| D、向NaAlO2溶液中通入过量CO2制Al(OH)3:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3_ |
有A、B、C、D、E五块金属片,进行如下实验:
①A、B用导线相连后,同时浸入稀H2SO4溶液中,A极为负极;
②C、D用导线相连后,同时浸入稀H2SO4溶液中,电流由D→导线→C;
③A、C相连后,同时浸入稀H2SO4溶液中,C极产生大量气泡;
④B、D相连后,同时浸入稀H2SO4溶液中,D极发生氧化反应;
⑤用惰性电极电解含B离子和E离子的溶液,E先析出.
据此,判断五种金属的活动性顺序是( )
①A、B用导线相连后,同时浸入稀H2SO4溶液中,A极为负极;
②C、D用导线相连后,同时浸入稀H2SO4溶液中,电流由D→导线→C;
③A、C相连后,同时浸入稀H2SO4溶液中,C极产生大量气泡;
④B、D相连后,同时浸入稀H2SO4溶液中,D极发生氧化反应;
⑤用惰性电极电解含B离子和E离子的溶液,E先析出.
据此,判断五种金属的活动性顺序是( )
| A、A>B>C>D>E |
| B、A>C>D>B>E |
| C、C>A>B>D>E |
| D、B>D>C>A>E |
下列说法中,正确的是( )
| A、能发生银镜反应的化合物一定是醛 |
| B、甲醛、乙酸、甲酸甲酯具有相同的最简式 |
C、C2H5OH和 具有相同的官能团,具有相同的化学性质 具有相同的官能团,具有相同的化学性质 |
| D、分子内有苯环和羟基的化合物一定是酚类 |
下列反应的离子方程式表示正确的是( )
| A、澄清石灰水中通入过量二氧化碳:OH-+CO2═HCO3- |
| B、铜片跟三氯化铁溶液反应:Fe3++Cu═Cu2++Fe2+ |
| C、漂白粉溶液中通入少量SO2:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO |
| D、Fe3O4与稀HNO3反应:Fe3O4+8H+═Fe2++2Fe3++4H2O |
在密闭容器中的一定量混合气体发生反应:xA(g)+yB(g)?zC(g),平衡时测得:c(A)为0.5mol/L,保持温度不变,将容器的容积扩大为原来的2倍,达到新平衡时测得c(A)为0.22mol/L.下列有关判断对的是( )
| A、x+y>z |
| B、化学反应速率将比原来的更快 |
| C、A、B的转化率减小 |
| D、混合气体的平均摩尔质量变小 |
下列除杂(括号内为杂质)有关操作,其中正确的是( )
| A、苯 (苯酚)--加入适量浓溴水,过滤 |
| B、NO (NO2)--通过水洗、干燥后,用向下排空气法收集 |
| C、乙烷 (乙烯)--让气体通过盛有酸性高锰酸钾溶液的洗气瓶 |
| D、乙醇 (乙酸)--加足量CaO固体,蒸馏 |
将1.12g铁粉加入25mL2mol/L的FeCl3溶液中,充分反应后,其结果是( )
| A、铁恰好将Fe3+全部还原 |
| B、往反应后溶液中滴入KSCN溶液,不显红色 |
| C、溶液变为浅绿色 |
| D、Fe2+和Fe3+物质的量之比为6:1 |