题目内容
3.要配制物质的量浓度约为2mol/L NaOH溶液100mL,下面的操作中,正确的是( )| A. | 称取8 g NaOH固体,放入250 mL烧杯中,用100 mL量筒量取100 mL蒸馏水,加入烧杯中,同时不断搅拌至固体溶解 | |
| B. | 称取8 g NaOH固体,放入100 mL量筒中,边搅拌,边慢慢加入蒸馏水,待固体完全溶解后用蒸馏水稀释至100 mL | |
| C. | 称取8 g NaOH固体,放入100 mL容量瓶中,加入适量蒸馏水,振荡容量瓶使固体溶解,再加入水到刻度,盖好瓶塞,反复摇匀 | |
| D. | 用100 mL量筒量取40 mL 5 mol/L NaOH溶液,倒入250 mL烧杯中,再用同一量筒量取60 mL蒸馏水,不断搅拌下,慢慢倒入烧杯中 |
分析 A.在100mL水中溶解8gNaOH固体,溶液的体积将大于100mL;
B.量筒只能用来量取液体,不能用来溶解固体;
C.容量瓶只能用来配制溶液,不能用来稀释或溶解药品;
D.根据两种溶液中含有溶质的物质的量是否相等判断.
解答 解:A.100mL水中溶解8gNaOH固体后,溶液的体积将大于100mL,所得溶液浓度小于2mol/L,故A错误;
B.溶解氢氧化钠固体应该在烧杯中进行,量筒只能用来量取液体,不能用来溶解固体,故B错误;
C.容量瓶只能用来配制溶液,不能用来稀释或溶解药品,故C错误;
D.100mL 2mol•L-1 的NaOH溶液含有氢氧化钠的物质的量是0.2mol,40mL5mol•L-1的NaOH溶液含有氢氧化钠的物质的量是0.2mol,两种溶液溶质的物质的量相等,所以能配制物质的量浓度约为2mol•L-1 NaOH溶液100mL,故D正确;
故选D.
点评 本题考查配制一定物质的量浓度的溶液,为高频考点,题目难度不大,明确配制步骤为解答关键,注意配制溶液的体积不等于水的体积,为易错点,试题培养了学生的化学实验能力.

练习册系列答案
相关题目
7.下列反应的离子方程式书写正确的是( )
| A. | 钠和水反应2Na+H2O═2Na++OH-+H2↑ | |
| B. | 氯化镁溶液加入氨水:Mg2++2OH-═Mg(OH)2↓ | |
| C. | 氯气与水反应:Cl2+H2O?H++Cl-+HClO | |
| D. | 氢氧化钡与稀硫酸反应:Ba2++SO42-═BaSO4↓ |
5.胃酸过多会损伤胃粘膜,使人感觉不适,抑酸剂就是为减少胃内盐酸的量而特制的,下列物质不可做抑酸剂的是( )
| A. | NaHCO3 | B. | NaAl(OH)2CO3 | C. | Mg(OH)2 | D. | BaCO3 |
12.下列实验现象的描述中不正确的是( )
| A. | 铁丝在空气中燃烧,火星四射,产生红棕色的烟 | |
| B. | 硫在氧气中燃烧发出明亮的蓝紫色火焰 | |
| C. | 在试管中加热铜绿有黑色固体生成 | |
| D. | 人造丝在酒精灯的火焰上灼烧会产生烧焦羽毛的气味 |
15.在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应:X(g)+Y(g)?2Z(g)△H<0,一段时间后达到平衡.反应过程中测定的数据如表:下列说法不正确的是( )
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 012 | 011 | 010 | 010 |
| A. | 反应前2min的平均速率v(Z)=2.0×10-5 mol•L-1•min-1 | |
| B. | 其他条件不变,降低温度,反应达到新平衡前:v(逆)>v(正) | |
| C. | 该温度下此反应的平衡常数:K=1.44 | |
| D. | 保持其他条件不变,起始时向容器充入0.32 mol气体X和0.32mol气体Y,到达平衡时,n(Z)=0.024mol |
12.下列有关化学用语表示正确的是( )
| A. | 质量数为35的氯原子:${\;}_{35}^{17}$Cl | |
| B. | NH4Cl的电子式: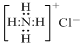 | |
| C. | NaHCO3的水解:HCO3-+H2O?CO32-+H3O+ | |
| D. | 天然橡胶的结构简式: |
13.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 5.6gFe在氧气中燃烧,完全反应时转移电子数为0.3NA | |
| B. | 1L 0.1mol•L-1AlC13中所含Al3+离子数小于0.1NA | |
| C. | 1LpH=1的H2SO4溶液中含有的H+数为0.2NA | |
| D. | 常温下,1.7gNH3和3.65gHCl混合后,气体分子数为0.2NA |