题目内容
1.下列说法正确的是:(NA表示阿伏加德罗常数的值)( )| A. | 28g氮气所含有的原子数目为NA | |
| B. | 6g金属镁变成镁离子时失去的电子数目为为NA | |
| C. | 标准状况下,22.4L任何气体所含分子数都约为NA | |
| D. | 50mL 1mol/L NaCl溶液所含的Cl-物质的量0.5NA |
分析 A.依据n=$\frac{m}{M}$计算物质的量结合分子式计算原子数;
B.依据n=$\frac{m}{M}$计算物质的量,结合镁最外层电子数为2分析;
C.标准状况下,22.4L任何气体所含分子的物质的量为1mol;
D.根据n=cV,进行计算求解.
解答 解:A.依据n=$\frac{m}{M}$计算物质的量=$\frac{28g}{28g/mol}$=1mol,结合分子式计算原子数为2NA ,故A错误;
B.依据n=$\frac{m}{M}$计算物质的量=$\frac{6g}{24g/mol}$=0.25mol,结合镁最外层电子数为2,6g金属镁变成镁离子时失去的电子数目为0.5NA,故B错误;
C.标准状况下,22.4L任何气体所含分子的物质的量为1mol,所以分子数约为NA,故C正确;
D.n=cV=0.05×1=0.05mol,故D错误;
故选C.
点评 本题考查阿伏加德罗常数的相关计算,题目难度不大,注意物质的组成、结构、性质以及相关物质的量的转化.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.放射性同位素钬16667Ho 的原子核内的中子数是( )
| A. | 99 | B. | 67 | C. | 32 | D. | 166 |
12.下列反应中,硫酸既表现出强氧化性,又表现出酸性的是( )
| A. | 稀硫酸与锌粒反应生成气体 | B. | 浓硫酸使铁、铝钝化 | ||
| C. | 浓硫酸与铜反应加热反应产生SO2 | D. | 浓硫酸和木炭在加热条件下反应 |
9.2SO2(g)+O2(g)$?_{△}^{催化剂}$2SO3(g)是制备硫酸过程中的一步重要反应,下列叙述正确的是( )
| A. | 催化剂不会改变该反应的逆反应速率 | |
| B. | 增大SO2(g)的浓度,逆反应速率会减小 | |
| C. | 该反应是放热反应,降低温度将缩短反应达到平衡的时间 | |
| D. | 在t1、t2时刻,SO3(g)的浓度分别是c1,c2,则时间间隔t1~t2内,SO3(g)生成的平均速率为v=$\frac{{c}_{2}-{c}_{1}}{{t}_{2}-{t}_{1}}$ |
16.某课外兴趣小组对H2O2的分解速率做了如下实验探究.
(1)下表是该小组研究影响过氧化氢(H2O2)分解速率的因素时采集的一组数据.表中数据为在不同条件下用10mL H2O2制取15OmLO2所需的时间(秒).
①上述实验结果体现了温度、催化剂、浓度等因素对过氧化氢分解速率的影响;
②从上述影响过氧化氢分解速率的因素中任选一个,说明该因素对化学反应速率的影响温度升高化学反应速率加快;反应物浓度增大化学反应速率加快;使用合适的催化剂化学反应速率加快.
(2)某温度时,在一个2L的密闭容器中,M、N、W三种气体的物质的量随时间的变化曲线如图所示.根据图中数据.试填写下列空白:
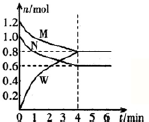
①该反应的化学方程式为M+N?2W.
②从开始至4min,N的平均反应速率为0.05mol/(L•min);4min 末M的转化率为33.3%.
(1)下表是该小组研究影响过氧化氢(H2O2)分解速率的因素时采集的一组数据.表中数据为在不同条件下用10mL H2O2制取15OmLO2所需的时间(秒).
| 浓度 时间(秒) 反应条件 | 30%H2O2 | 15%H2O2 | 10%H2O2 | 5%H2O2 |
| 无催化剂、不加热 | 几乎不反应 | 几乎不反应 | 几乎不反应 | 几乎不反应 |
| 无催化剂、加热 | 360 | 480 | 540 | 720 |
| MnO2催化剂、加热 | 10 | 25 | 60 | 120 |
②从上述影响过氧化氢分解速率的因素中任选一个,说明该因素对化学反应速率的影响温度升高化学反应速率加快;反应物浓度增大化学反应速率加快;使用合适的催化剂化学反应速率加快.
(2)某温度时,在一个2L的密闭容器中,M、N、W三种气体的物质的量随时间的变化曲线如图所示.根据图中数据.试填写下列空白:

①该反应的化学方程式为M+N?2W.
②从开始至4min,N的平均反应速率为0.05mol/(L•min);4min 末M的转化率为33.3%.
10.下列叙述正确的是( )
| A. | 将5.85gNaCl晶体溶入100mL水中,制得0.1mol/L的NaCl溶液 | |
| B. | 将25g无水硫酸铜粉末溶于水制成100mL溶液,其浓度为1mol/L | |
| C. | 将0.2mol/L稀硫酸与等质量的蒸馏水混合后,浓度大于0.1mol/L | |
| D. | 将1体积1mol/L的稀硫酸用水稀释到5体积,溶液的浓度为0.2mol/L |
4.光导纤维的主要化学成分( )
| A. | 二氧化硅 | B. | 硅 | C. | 硅酸 | D. | 硅酸钠 |