题目内容
(12分)实验室用辉铜矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质)制备碱式碳酸铜的主要实验流程如下。
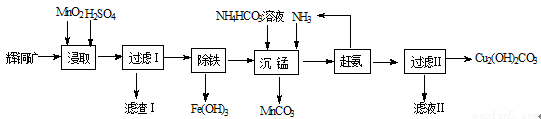
(1)滤渣Ⅰ的成分为MnO2、单质S和 (写化学式);硫酸浸取时,Cu2S被MnO2氧化的化学方程式为 。
(2)浸取时,Fe2O3溶于硫酸的离子方程式为 ;研究发现若先除铁再浸取,浸取速率明显变慢,其可能原因是 。
(3)“赶氨”时,最适宜的操作方法是 。
(4)滤液Ⅱ经蒸发结晶得到的盐主要是 (写化学式)。
(1)SiO2 (2分);2MnO2 + Cu2S + 4H2SO4 = 2MnSO4 + 2CuSO4 +S+4H2O(2分)
(2)Fe2O3+6H+=2Fe3++3H2O (2分);Fe3+可催化Cu2S被MnO2氧化(2分)
(3)将溶液加热(2分)(4)(NH4)2SO4(2分)。
【解析】
试题分析:由于辉铜矿的主要成分为Cu2S,含少量Fe2O3、SiO2等杂质,所以向其中加入MnO2、H2SO4时会发生氧化还原反应2MnO2 + Cu2S + 4H2SO4 = 2MnSO4 + 2CuSO4 +S+4H2O,产生单质S、MnSO4、CuSO4 、H2O,酸性氧化物SiO2及过量的MnO2和产生的S都不能在水中溶解,因此过滤会除去;(2)浸取时,Fe2O3溶于硫酸发生离子反应:Fe2O3+6H+=2Fe3++3H2O;研究发现若先除铁再浸取,浸取速率明显变慢,其可能原因是Fe3+可催化Cu2S被MnO2氧化;(3)由于气体在溶液中的溶解度会随着温度的升高而降低,所以“赶氨”时,最适宜的操作方法是将溶液加热;(4)由于在溶液中存在NH4+、CO32-、SO42-、OH-、Cu2+;由于CO32-、OH-、Cu2+以Cu2(OH)2CO3存在,所以滤液Ⅱ经蒸发结晶得到的盐主要是(NH4)2SO4。
考点:考查物质制取过程中反应条件的控制、离子方程式和化学方程式的书写及物质的成分的确定的知识。

 阅读快车系列答案
阅读快车系列答案 BCl3空间形状为 (用文字描述)。
BCl3空间形状为 (用文字描述)。 键数目为 。
键数目为 。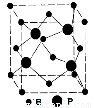
 的说法正确的是
的说法正确的是