题目内容
烧过菜的铁锅未及时洗去含有NaCl的残液,过一段时间便出现红棕色的铁锈斑点,已知该锈斑为Fe(OH)3失水的产物.铁锅的锈蚀主要属于 (填“析氢”或“吸氧”)腐蚀.
(1)请你表示此时Fe被腐蚀的电极反应式:负极 ,正极 .
(2)Fe2+和NaOH溶液反应生成Fe(OH)2的离子方程式
(3)发生原电池反应生成Fe(OH)2的总反应式为
(4)Fe(OH)2与O2和水反应转化为Fe(OH)3,然后进一步转化为铁锈的化学方程式: .
(1)请你表示此时Fe被腐蚀的电极反应式:负极
(2)Fe2+和NaOH溶液反应生成Fe(OH)2的离子方程式
(3)发生原电池反应生成Fe(OH)2的总反应式为
(4)Fe(OH)2与O2和水反应转化为Fe(OH)3,然后进一步转化为铁锈的化学方程式:
考点:金属的电化学腐蚀与防护
专题:电化学专题
分析:(1)铁发生吸氧腐蚀,负极发氧化反应,正极氧气得电子被还原;
(2)Fe2+和OH-应生成Fe(OH)2;
(3)总反应为铁、氧气和水反应生成Fe(OH)2;
(4)Fe(OH)2与O2和水反应转化为Fe(OH)3,Fe(OH)3部分失水可生成铁锈.
(2)Fe2+和OH-应生成Fe(OH)2;
(3)总反应为铁、氧气和水反应生成Fe(OH)2;
(4)Fe(OH)2与O2和水反应转化为Fe(OH)3,Fe(OH)3部分失水可生成铁锈.
解答:
解:铁被氧化生成Fe(OH)3,说明反应液呈中性或碱性,则应发生吸氧腐蚀,故答案为:吸氧;
(1)铁发生吸氧腐蚀,负极发氧化反应,电极方程式为2Fe=2Fe2++4e-,正极氧气得电子被还原,电极方程式为2H2O+O2+4e-=4OH-,
故答案为:2Fe=2Fe2++4e-;2H2O+O2+4e-=4OH-;
(2)Fe2+和OH-应生成Fe(OH)2,反应的离子方程式为Fe2++2OH-=Fe(OH)2,故答案为:Fe2++2OH-=Fe(OH)2;
(3)总反应为铁、氧气和水反应生成Fe(OH)2,反应的方程式为2Fe+2H2O+O2=2Fe(OH)2,
故答案为:2Fe+2H2O+O2=2Fe(OH)2;
(4)Fe(OH)2与O2和水反应转化为Fe(OH)3,Fe(OH)3部分失水可生成铁锈,涉及反应有4Fe(OH)2+2H2O+O2=4Fe(OH)3;2Fe(OH)3=Fe2O3.xH2O+(3-x)H2O,
故答案为:4Fe(OH)2+2H2O+O2=4Fe(OH)3;2Fe(OH)3=Fe2O3.xH2O+(3-x)H2O.
(1)铁发生吸氧腐蚀,负极发氧化反应,电极方程式为2Fe=2Fe2++4e-,正极氧气得电子被还原,电极方程式为2H2O+O2+4e-=4OH-,
故答案为:2Fe=2Fe2++4e-;2H2O+O2+4e-=4OH-;
(2)Fe2+和OH-应生成Fe(OH)2,反应的离子方程式为Fe2++2OH-=Fe(OH)2,故答案为:Fe2++2OH-=Fe(OH)2;
(3)总反应为铁、氧气和水反应生成Fe(OH)2,反应的方程式为2Fe+2H2O+O2=2Fe(OH)2,
故答案为:2Fe+2H2O+O2=2Fe(OH)2;
(4)Fe(OH)2与O2和水反应转化为Fe(OH)3,Fe(OH)3部分失水可生成铁锈,涉及反应有4Fe(OH)2+2H2O+O2=4Fe(OH)3;2Fe(OH)3=Fe2O3.xH2O+(3-x)H2O,
故答案为:4Fe(OH)2+2H2O+O2=4Fe(OH)3;2Fe(OH)3=Fe2O3.xH2O+(3-x)H2O.
点评:本题考查了金属的电化学腐蚀及电解池原理,为高频考点,侧重于学生的分析能力的考查,注意把握钢铁所处环境的酸碱性即可确定其电化学腐蚀类型,难度不大.

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目
下列叙述中,正确的是( )
| A、甲苯既可使溴的四氯化碳溶液褪色,也可使酸性高锰酸钾溶液褪色 |
| B、有机物2-溴丁烷的消去产物有两种 |
| C、有机物A(C4H6O2)能发生加聚反应,可推知A的结构一定是CH2═CH-COOCH3 |
| D、可用溴水鉴别1-己烯、四氯化碳和乙酸 |
下列与有机物的结构、性质有关的叙述正确的是( )
| A、硫酸铵、硫酸铜和乙醇均能使蛋白质变性 |
| B、甲烷、乙烯和苯在工业上都可以通过石油分馏得到 |
| C、用新制氢氧化铜悬浊液可以鉴别葡萄糖和乙酸 |
| D、甲苯的一氯代物有三种 |
1mol乙烯与Cl2完全加成后再与Cl2发生最大程度的取代,两个过程共需Cl2( )
| A、3 mol |
| B、4 mol |
| C、5 mol |
| D、6 mol |
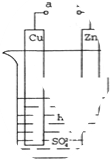 原电池是化学对人类的一项重大贡献.
原电池是化学对人类的一项重大贡献.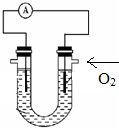 C、N、S的单质和化合物在工农业生产中有重要的应用.
C、N、S的单质和化合物在工农业生产中有重要的应用.