题目内容
2.某酸碱指示剂(HIn)在水溶液中存在以下平衡:HIn(aq)?H++In-(aq)
(红色) (蓝色)
下列物质的溶液中,能使指示剂显蓝色的是( )
| A. | 稀硫酸 | B. | 氯化铝溶液 | C. | 稀氨水 | D. | 饱和食盐水 |
分析 能使指示剂显蓝色,应使c(HIn)<c(In-),则加入物质应使平衡向正反应方向移动,所以加入溶液应呈碱性,以此解答该题.
解答 解:能使指示剂显蓝色,应使c(HIn)<c(In-),则加入物质应使平衡向正反应方向移动,所以加入溶液应呈碱性,AB为酸性溶液,可使平衡向逆反应方向移动,而C溶液呈碱性,可使平衡向正反应方向移动,D为中性溶液,平衡不移动,
故选C.
点评 本题考查化学平衡的影响因素,题目难度不大,注意根据颜色的变化判断平衡移动的移动方向,结合外界条件对平衡移动的影响分析.

练习册系列答案
相关题目
16.下列四幅图的相关说法正确的是( )
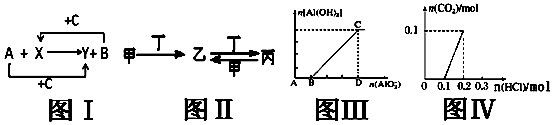

| A. | 关于图Ⅰ,已知C是氧气,X、Y是化合物,则A是钠,B是氢气 | |
| B. | 关于图Ⅱ,已知甲、乙、丙均含有相同的某种元素,若甲为NaOH溶液,则丁可能是CO2 | |
| C. | 关于图Ⅲ,表示NaAlO2溶液逐滴加入到NaOH溶液中,n(Al(OH)3)和n(AlO2-)之间的关系图象 | |
| D. | 关于图Ⅳ,表示各含0.1mol苏打和NaOH混合液中逐滴加入含溶质0.2mol的盐酸的关系图象 |
13.下列依据热化学方程式得出的结论正确的是( )
| A. | 已知2H2(g)+O2(g)=2H2O(g)△H=-483.6 kJ•mol--1,则氢气的燃烧热为241.8 kJ•mol-1 | |
| B. | 已知2C(s)+2O2(g)=2CO2(g)△H=a,2C(s)+O2(g)=2CO(g)△H=b,则a>b | |
| C. | 已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-57.3 kJ•mol-1,则含40.0 g NaOH的稀溶液与稀醋酸完全中和,放出的热量小于57.3 kJ | |
| D. | 已知P (白磷,s)=P (红磷,s)△H<0,则白磷比红磷稳定 |
17.下列各组微粒能大量共存,当加入相应试剂后会发生化学变化,且发生反应的离子方程式书写正确的是( )
| 选项 | 微粒组 | 所加试剂 | 离子方程式 |
| A | NH4+、Fe2+、SO42- | 少量Ba(OH)2溶液 | 2NH4++SO42-+Ba2++2OH-═BaSO4↓+2NH3•H2O |
| B | Mg2+、Cl-、HCO3- | 过量NaOH溶液 | Mg2++2HCO3-+4OH-═Mg(OH)2↓+2CO32-+2H2O |
| C | Fe2+、NO3-、HSO3- | NaHSO4溶液 | HSO3-+H+═SO2↑+H2O |
| D | K+、CO32-、NH3•H2O | 通入少量CO2 | CO32-+CO2+2H2O═2HCO3- |
| A. | A | B. | B | C. | C | D. | D |
14.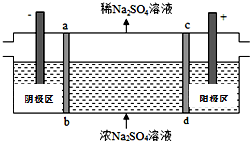 三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42-可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室.下列叙述正确的是( )
三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42-可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室.下列叙述正确的是( )
 三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42-可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室.下列叙述正确的是( )
三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42-可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室.下列叙述正确的是( )| A. | 通电后中间隔室的SO42-离子向正极迁移,正极区溶液碱性增强 | |
| B. | 该法在处理含Na2SO4废水时可以得到NaOH和H2SO4产品 | |
| C. | 阴极区溶液pH降低,阳极区溶液pH升高 | |
| D. | 当电路中通过1mol电子的电量时,会有0.5mol的O2生成 |
11.下列说法中正确的是( )
| A. | 将322 g Na2SO4•10H2O溶于1 L水中,所得溶液的物质的量浓度为1 mol/L | |
| B. | 将含2 mol H2SO4的溶液加水稀释到2 L,所得溶液中H2SO4的物质的量浓度为1 mol/L | |
| C. | 将1 L 18.4 mol/L的H2SO4溶液加入1 L水中,所得溶液的物质的量浓度为9.2 mol/L | |
| D. | 将336 mL HCl气体溶于300 mL水,所得溶液的物质的量浓度为0.05 mol/L |