题目内容
下列离子方程式书写正确的是( )
| A、盐酸与碳酸钡反应:CO32-+2H+═CO2↑+H2O |
| B、往硫酸铜溶液中滴加氢氧化钡溶液:Ba2++2OH-+Cu2++SO42-═BaSO4↓+Cu(OH)2↓ |
| C、稀硫酸溶液与氨水反应:H++OH-═H2O |
| D、铁与稀盐酸反应:2Fe+6H+═2Fe3++3H2↑ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.碳酸钡在离子反应中应保留化学式;
B.反应生成硫酸钡和氢氧化铜;
C.一水合氨在离子反应中应保留化学式;
D.反应生成氯化亚铁和氢气.
B.反应生成硫酸钡和氢氧化铜;
C.一水合氨在离子反应中应保留化学式;
D.反应生成氯化亚铁和氢气.
解答:
解:A.盐酸与碳酸钡反应的离子反应为CaCO3+2H+═CO2↑+H2O+Ca2+,故A错误;
B.往硫酸铜溶液中滴加氢氧化钡溶液的离子反应为Ba2++2OH-+Cu2++SO42-═BaSO4↓+Cu(OH)2↓,故B正确;
C.稀硫酸溶液与氨水反应的离子反应为H++NH3.H2O═H2O+NH4+,故C错误;
D.铁与稀盐酸反应的离子反应为Fe+2H+═Fe2++H2↑,故D错误;
故选B.
B.往硫酸铜溶液中滴加氢氧化钡溶液的离子反应为Ba2++2OH-+Cu2++SO42-═BaSO4↓+Cu(OH)2↓,故B正确;
C.稀硫酸溶液与氨水反应的离子反应为H++NH3.H2O═H2O+NH4+,故C错误;
D.铁与稀盐酸反应的离子反应为Fe+2H+═Fe2++H2↑,故D错误;
故选B.
点评:本题考查离子反应方程式的书写,为高频考点,把握发生的化学反应及离子反应的书写方法为解答的关键,侧重复分解反应的离子反应书写,综合性较强,较好的训练学生思维的严密性,有利于分析能力的培养,选项D为解答的易错点,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
反应SO2(g)+NO2(g)?NO(g)+SO3(g)在恒温恒容下建立平衡后,通入一定量的O2,下列说法正确的是( )
| A、平衡左移,达到平衡时容器内压强增大 |
| B、平衡右移,达到平衡时容器内压强不变 |
| C、平衡不移动,达到平衡时容器内压强增大 |
| D、平衡右移,SO2的转化率提高 |
下列有关实验的说法正确的是( )
| A、将FeCl3溶液加热至沸腾,溶液由黄色变为红褐色 |
B、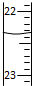 滴定达终点时,如图滴定管的正确读数为23.65 mL |
| C、向AgI悬浊液中滴加少量NaCl溶液,沉淀转化为白色 |
| D、测定溶液的pH时,应先将pH试纸润湿,然后进行检测 |
根据X
氧化物
强酸或强碱,下列说法不正确是( )
①X一定是单质;②反应Ⅱ一定是化合反应;③若强酸为HNO3,氧化物一定是酸性氧化物;④若强碱为NaOH,氧化物一定是Na2O.
| 反应Ⅰ |
| 反应Ⅱ |
①X一定是单质;②反应Ⅱ一定是化合反应;③若强酸为HNO3,氧化物一定是酸性氧化物;④若强碱为NaOH,氧化物一定是Na2O.
| A、①③ | B、②③ | C、②③④ | D、全部 |
下列离子方程式正确的是( )
| A、Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O |
| B、用醋酸除去水垢:CaCO3+2H+=Ca2++H2O+CO2↑ |
| C、NO2与水的反应:3NO2+H2O=2NO3-+NO+2H+ |
| D、等体积、等浓度的Ca(HCO3)2溶液和NaOH溶液混合:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O |
下列各组离子中,在给定条件下可能大量共存的是( )
| A、在pH=2的溶液中:NH4+、K+、ClO-、Cl- |
| B、加入铝粉有氢气生成的溶液:CO32-、Cl-、K+、Na+ |
| C、由水电离产生的c(OH-)=1×10-15mol/L的溶液:Fe2+、Na+、NO3-、Cl- |
| D、加入NH4HCO3有气体生成的无色溶液:Cl-、Cu2+、H+、SO42- |
 在如图所示的电解装置中:
在如图所示的电解装置中: