题目内容
下列各组物质不属于同素异形体的是( )
| A、.H2O和H2O2 |
| B、O2和O3 |
| C、金刚石和石墨 |
| D、红磷和白磷 |
考点:同素异形体
专题:原子组成与结构专题
分析:由同种元素形成的不同种单质互为同素异形体,互为同素异形体的物质要符合以下两个条件:同种元素形成,不同单质;据此进行分析判断.
解答:
解:判断同素异形体的关键把握两点:①同种元素形成,②不同单质.
A、H2O和H2O2是化合物,不是单质,故H2O和H2O2不属于同素异形体,故A错误;
B、O2和O3都是由氧元素形成的不同物质,都是单质,互为同素异形体,故B正确;
C、金刚石和石墨都是由碳元素形成的不同物质,都是单质,互为同素异形体,故C正确;
D、红磷和白磷都是由磷元素形成的不同物质,都是单质,互为同素异形体,故D正确.
故选A.
A、H2O和H2O2是化合物,不是单质,故H2O和H2O2不属于同素异形体,故A错误;
B、O2和O3都是由氧元素形成的不同物质,都是单质,互为同素异形体,故B正确;
C、金刚石和石墨都是由碳元素形成的不同物质,都是单质,互为同素异形体,故C正确;
D、红磷和白磷都是由磷元素形成的不同物质,都是单质,互为同素异形体,故D正确.
故选A.
点评:本题难度不大,判断是否互为同素异形体的关键要把握两点:①同种元素形成,②不同单质,这是解决此类题的关键之所在.

练习册系列答案
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案
相关题目
下列离子方程式不正确的是( )
| A、向沸水中滴加饱和氯化铁溶液,加热至溶液呈红褐色:Fe3++3H2O?Fe(OH)3(胶体)+3H+ |
| B、常温下Cl2与NaOH溶液反应:Cl2+2OH-=Cl-+ClO-+H2O |
| C、小苏打与醋酸溶液混合:HCO3-+CH3COOH=CH3COO-+CO2↑+H2O |
| D、向Ba(OH)2溶液中滴入过量的NaHSO4溶液:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
分类法是一种行之有效、简单易行的科学方法.某同学用下表所示的形式对所学知识进行分类,其中甲与乙、丙、丁是包含关系的组合的是( )
| 选项 | 甲 | 乙、丙、丁 |
| ① | 干燥剂 | 浓硫酸、石灰石、碱石灰 |
| ② | 合金 | 不锈钢、青铜、生铁 |
| ③ | 胶体 | 稀豆浆、血液、淀粉溶液 |
| ④ | 腐蚀品 | 浓硫酸、烧碱、硝酸 |
| ⑤ | 碱性氧化物 | 过氧化钠、氧化镁、氧化铁 |
| ⑥ | 电解质 | 水、冰醋酸、四氯化碳 |
| A、②③④ | B、①②③④ |
| C、①②④⑤ | D、①②④⑥ |
下列物质中,属于非电解质的是( )
| A、食盐 | B、盐酸 | C、蔗糖 | D、磷酸钠 |
Al2(SO4)3、K2SO4、KAl(SO4)2的混合溶液100mL中,如果SO42-的浓度为0.8mol/L,当加入2mol/L的KOH溶液100mL时,生成沉淀恰好溶解,则原混合物中K+的物质的量浓度是( )
| A、0.2mol/L |
| B、0.1mol/L |
| C、0.45mol/L |
| D、0.225mol/L |
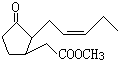 如图是茉莉酮酸酯的结构简式,有关该物质的说法正确的是( )
如图是茉莉酮酸酯的结构简式,有关该物质的说法正确的是( )| A、该有机物能使酸性高锰酸钾溶液褪色 |
| B、该有机物分子中含有三个亚甲基(-CH2-) |
| C、该有机物可以发生银镜反应 |
| D、该物质在酸性条件下的水解比在碱性条件下的水解程度大 |
对于可逆反应N2+3H2?2NH3,下列说法可以说明反应已达到平衡状态的是( )
| A、N2、H2、NH3的浓度相等 |
| B、N2、H2、NH3的浓度不再发生变化 |
| C、反应停止 |
| D、N2、H2、NH3在容器中共存 |
