题目内容
6.氮、碳都是重要的非金属元素,含氮、碳元素的物质在工业生产中有重要的应用.一定条件下,铁可以和CO2发生反应:Fe(s)+CO2(g)?FeO(s)+CO(g),已知该反应的平衡常数K与温度T的关系如图所示.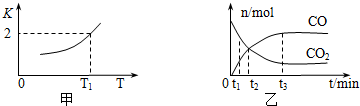
①该反应的逆反应是放热(填“吸热”或“放热”)反应.该反应的平衡常数表达式为$\frac{c(CO)}{c(C{O}_{2})}$
②T℃、P pa压强下,在体积为VL的容器中进行反应,下列能说明反应达到平衡状态的是AD.
A.混合气体的平均相对分子质量不再变化;
B.容器内压强不再变化;
C.v正(CO2)=v逆(FeO)
D.混合气体的密度不再变化
③T1温度下,向体积为V L的密闭容器中加入足量铁粉并充入一定量的CO2,反应过程中CO和CO2物质的量与时间的关系如图乙所示.则CO2的平衡转化率为$\frac{2}{3}$,平衡时混合气体的密度与起始时气体的密度之比为$\frac{25}{33}$.
分析 (1)图象甲中平衡常数曲线随温度升高增大,说明正反应为吸热反应,逆向为放热反应;平衡常数为产物浓度系数次幂的乘积与反应物浓度系数次幂的乘积的比值;(2)当反应达到平衡状态时,正、逆反应速率相等(同种物质),各物质的浓度、含量不再改变,以及由此衍生的一些物理量也不变,以此进行判断;
(3)T1温度下,向体积为V L的密闭容器中加入足量铁粉并充入一定量的CO2,平衡常数为2,设二氧化碳起始量为x,变化量为y,
Fe(s)+CO2(g)?FeO(s)+CO(g),
起始量 x 0
变化量 y y
平衡量 x-y y
平衡常数K=$\frac{y}{x-y}$=2,所以$\frac{y}{x}$=$\frac{2}{3}$,
二氧化碳转化率$\frac{y}{x}$=$\frac{2}{3}$,由此分析解答.
解答 解:(1)图象甲中平衡常数曲线随温度升高而增大,说明正反应为吸热反应,逆向为放热反应,平衡常数为产物浓度系数次幂的乘积与反应物浓度系数次幂的乘积的比值,由于Fe和FeO为固体,不能写在化学平衡常数表达式中,所以K=$\frac{c(CO)}{c(C{O}_{2})}$,
故答案为:放热;$\frac{c(CO)}{c(C{O}_{2})}$;
(2)Fe(s)+CO2(g)?FeO(s)+CO(g),反应前后是气体体积不变的放热反应,
A、反应前后气体物质的量不变,气体质量发生变化,混合气体的平均相对分子质量不再变化,说明反应达到平衡状态,A正确;
B、反应前后气体体积不变,容器内压强始终不发生变化,不能说明反应达到平衡状态,故B错误;
C、氧化亚铁是固体,不能表示反应速率,故C错误;
D、混合气体的密度不再变化,说明气体的质量不变反应达平衡状态,故D正确
故答案为:AD;
(3)T1温度下,向体积为V L的密闭容器中加入足量铁粉并充入一定量的CO2,平衡常数为2,设二氧化碳起始量为x,变化量为y,
Fe(s)+CO2(g)?FeO(s)+CO(g),
起始量 x 0
变化量 y y
平衡量 x-y y
平衡常数K=$\frac{y}{x-y}$=2,所以$\frac{y}{x}$=$\frac{2}{3}$,
二氧化碳转化率$\frac{y}{x}$=$\frac{2}{3}$,
平衡时混合气体的密度与起始时气体的密度之比为气体摩尔质量之比=$\frac{44(x-y)+28y}{x}$:44=$\frac{25}{33}$,
故答案为:$\frac{2}{3}$; $\frac{25}{33}$.
点评 本题考查化学平衡常数表达式,难度不大,注意纯固体纯液体不能写在化学平衡常数表达式中.

 名校课堂系列答案
名校课堂系列答案| A. | 浓硫酸、水 | B. | 饱和食盐水、浓H2SO4 | ||
| C. | 烧碱、石灰水 | D. | 无水CaCl2、烧碱 |
| A. | SO2 | B. | Ca(ClO)2 | C. | NaClO | D. | H2SO4(浓) |
| A. |  图除去CO2中的HCl | |
| B. |  图装置制备Fe(OH)2并能较长时间观察其颜色 | |
| C. |  图所示装置制取并收集干燥纯净的NH3 | |
| D. | 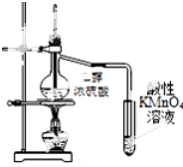 图证明CH3CH2OH发生消去反应生成了乙烯 |
| A. | Na+ H+ NO3- Fe2+ | B. | Ca2+ NO3- HCO3- OH- | ||
| C. | K+ H+ Cl- SO42- | D. | Fe3+ Cl- H+ CO32- |
| 实验编号 | HA物质的量浓度(mol•L-1) | NaOH物质的量浓度(mol•L-1) | 混合溶液的pH |
| ① | 0.1 | 0.1 | pH=9 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.2 | 0.1 | pH<7 |
(1)根据①组实验情况,分析混合溶液的pH=9的原因是H2O+A-?HA+OH-.(用反应的离子方程式表示),在该溶液中下列关系式正确的是(填序号字母)BD.
A.c(Na+)+c(H+)=c(OH-)+c(A-)+c(HA) B.c(Na+)=c(HA)+c(A-)
C.c(HA)+c(H+)=c(OH-)+c(Na+) D.c(Na+)+c(H+)=c(OH-)+c(A-)
(2)②组情况表明,c>0.2mol•L-1(选填“>”、“<”或“=”).混合溶液中离子浓度c(A-)=c(Na+)(选填“>”、“<”或“=”)
(3)从③组实验结果分析,说明溶液中离子浓度由大到小的顺序是c(A-)>c(Na+)>c(H+)>c(OH-).
| A. | 1.1 mol•l-1 | B. | 1.5mol•L-1 | C. | 2.4 mol•L-1 | D. | 无法确定 |
| A. | NaHSO4溶液与NaOH溶液混合 | B. | NH4Cl溶液与Ca(OH)2溶液混合 | ||
| C. | HNO3溶液与石灰乳混合 | D. | Na2HPO4溶液与NaOH溶液混合 |
| A. | 升高温度 | B. | 增加压强 | C. | 增大反应物的量 | D. | 使用催化剂 |