题目内容
按要求填空:
(1)写出下列物质在水溶液中的电离方程式:硫酸铝: ,碳酸氢钙: .
(2)现有以下物质:①NaCl溶液 ②干冰(固态的二氧化碳) ③冰醋酸(纯净的醋酸) ④铜 ⑤BaSO4固体 ⑥酒精 ⑦熔融的KNO3⑧氨水⑨盐酸 ⑩液氨 液态HCl
液态HCl NaOH固体
NaOH固体 Na2SO4?10H2O
Na2SO4?10H2O
其中能够导电的是 (填序号,下同);属于强电解质但在上述状态下不导电的是 ;属于非电解质的是
(3)某一反应体系中有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2.已知该反应中H2O2只发生如下过程:H2O2→O2,则该反应中的氧化剂和氧化产物分别是 ,若反应转移了0.3mol电子,则产生的气体在标准状况下体积为 L
(4)现有m g某气体,它由双原子分子构成,它的摩尔质量为M g?mol-1.若阿伏加德罗常数用NA表示,则:①m g该气体所含原子数 .
②标况下VL该气体溶于1L水中(不考虑反应),其溶液中溶质的质量分数为 _ _.
(1)写出下列物质在水溶液中的电离方程式:硫酸铝:
(2)现有以下物质:①NaCl溶液 ②干冰(固态的二氧化碳) ③冰醋酸(纯净的醋酸) ④铜 ⑤BaSO4固体 ⑥酒精 ⑦熔融的KNO3⑧氨水⑨盐酸 ⑩液氨
 液态HCl
液态HCl NaOH固体
NaOH固体 Na2SO4?10H2O
Na2SO4?10H2O其中能够导电的是
(3)某一反应体系中有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2.已知该反应中H2O2只发生如下过程:H2O2→O2,则该反应中的氧化剂和氧化产物分别是
(4)现有m g某气体,它由双原子分子构成,它的摩尔质量为M g?mol-1.若阿伏加德罗常数用NA表示,则:①m g该气体所含原子数
②标况下VL该气体溶于1L水中(不考虑反应),其溶液中溶质的质量分数为
考点:电离方程式的书写,阿伏加德罗常数,氧化还原反应,电解质与非电解质
专题:
分析:(1)硫酸铝和碳酸氢钙都是强电解质,在溶液中完全电离,电离方程式用等号;
(2)电解质:在水溶液中或熔融状态下能够导电的化合物;非电解质:在熔融状态和水溶液中都不能导电的化合物;
在水溶液中完全电离的是强电解质;部分电离的是弱电解质;
(3)氧化剂发生还原反应;还原剂发生氧化反应,生成氧化产物,根据元素的化合价变化进行分析判断;
由反应可知生成3mol气体转移6mol电子,以此进行计算;
(4)①由n=
计算气体物质的量,原子物质的量为气体分子2倍,再根据N=nNA计算原子数目;
②根据ω=
×100%计算出该溶液中溶质的质量分数.
(2)电解质:在水溶液中或熔融状态下能够导电的化合物;非电解质:在熔融状态和水溶液中都不能导电的化合物;
在水溶液中完全电离的是强电解质;部分电离的是弱电解质;
(3)氧化剂发生还原反应;还原剂发生氧化反应,生成氧化产物,根据元素的化合价变化进行分析判断;
由反应可知生成3mol气体转移6mol电子,以此进行计算;
(4)①由n=
| m |
| M |
②根据ω=
| m溶质 |
| m溶液 |
解答:
解:(1)硫酸铝为强电解质,在溶液中完全电离出硫酸根离子和铝离子,电离方程式为:Al2(SO4)3=2Al3++3SO42-,
碳酸氢钙为强电解质,在溶液中完全电离出碳酸氢根离子和钙离子,电离方程式为:Ca(HCO3)2=Ca2++2HCO3-,
故答案为:Al2(SO4)3=2Al3++3SO42-;Ca(HCO3)2=Ca2++2HCO3-;
(2)①NaCl溶液是混合物,能导电,既不是电解质也不是非电解质;
②干冰不能导电,且自身不能电离,是非电解质;
③冰醋酸不能导电,在水溶液中部分电离,能够导电,是弱电解质;
④铜金属单质,存在自由移动的电子,能导电,既不是电解质也不是非电解质;
⑤BaSO4固体不能导电,在熔融状态下能够导电,溶于水的部分完全电离,是强电解质;
⑥酒精不能导电,是非电解质;
⑦熔融的KNO3能导电,在水溶液中完全电离,是强电解质;
⑧氨水是混合物,能导电,既不是电解质也不是非电解质;
⑨盐酸是混合物,能导电,既不是电解质也不是非电解质;
⑩液氨不能导电,是非电解质;
 液态HCl不能导电,在水溶液中完全电离,是强电解质;
液态HCl不能导电,在水溶液中完全电离,是强电解质;
 NaOH固体不能导电,在水溶液中完全电离,是强电解质;
NaOH固体不能导电,在水溶液中完全电离,是强电解质;
 Na2SO4?10H2O不能导电,在水溶液中完全电离,是强电解质;
Na2SO4?10H2O不能导电,在水溶液中完全电离,是强电解质;
故能够导电的是①④⑦⑧⑨;属于强电解质但在上述状态下不导电的是⑤
 ;属于非电解质的是②⑥⑩,
;属于非电解质的是②⑥⑩,
故答案为:①④⑦⑧⑨;⑤
 ;②⑥⑩;
;②⑥⑩;
(3)H2O2 发生的过程:H2O2→O2中O元素化合价升高,因此H2O2 作还原剂,被氧化生成氧气,故氧气为氧化产物;
H2CrO4发生的过程:H2CrO4→Cr(OH)3中Cr元素化合价降低,因此H2CrO4作还氧化剂;
反应方程式为:2H2CrO4+3H2O2═2Cr(OH)3↓+3O2↑+2H2O,根据方程式可知:生成3mol气体转移6mol电子,则转移了0.3mol电子,则产生的气体的物质的量为
×3mol=0.15mol,即标准状况下的体积为22.4×0.15=3.36L;
故答案为:H2CrO4和O2,3.36;
(4)①mg气体的物质的量=
=
mol,由双原子分子构成,原子物质的量为气体分子2倍,故含有原子数目=
mol×2×NAmol-1=
,
故答案为:
;
②VL该气体的质量为
×Mg,1L水的质量约为1000g,则溶液的质量为(
+1000)g,则形成的溶液中溶质的质量分数为:ω=
×100%=
×100%=
×100%%,
故答案为:
×100%%.
碳酸氢钙为强电解质,在溶液中完全电离出碳酸氢根离子和钙离子,电离方程式为:Ca(HCO3)2=Ca2++2HCO3-,
故答案为:Al2(SO4)3=2Al3++3SO42-;Ca(HCO3)2=Ca2++2HCO3-;
(2)①NaCl溶液是混合物,能导电,既不是电解质也不是非电解质;
②干冰不能导电,且自身不能电离,是非电解质;
③冰醋酸不能导电,在水溶液中部分电离,能够导电,是弱电解质;
④铜金属单质,存在自由移动的电子,能导电,既不是电解质也不是非电解质;
⑤BaSO4固体不能导电,在熔融状态下能够导电,溶于水的部分完全电离,是强电解质;
⑥酒精不能导电,是非电解质;
⑦熔融的KNO3能导电,在水溶液中完全电离,是强电解质;
⑧氨水是混合物,能导电,既不是电解质也不是非电解质;
⑨盐酸是混合物,能导电,既不是电解质也不是非电解质;
⑩液氨不能导电,是非电解质;
 液态HCl不能导电,在水溶液中完全电离,是强电解质;
液态HCl不能导电,在水溶液中完全电离,是强电解质; NaOH固体不能导电,在水溶液中完全电离,是强电解质;
NaOH固体不能导电,在水溶液中完全电离,是强电解质; Na2SO4?10H2O不能导电,在水溶液中完全电离,是强电解质;
Na2SO4?10H2O不能导电,在水溶液中完全电离,是强电解质;故能够导电的是①④⑦⑧⑨;属于强电解质但在上述状态下不导电的是⑤
 ;属于非电解质的是②⑥⑩,
;属于非电解质的是②⑥⑩,故答案为:①④⑦⑧⑨;⑤
 ;②⑥⑩;
;②⑥⑩;(3)H2O2 发生的过程:H2O2→O2中O元素化合价升高,因此H2O2 作还原剂,被氧化生成氧气,故氧气为氧化产物;
H2CrO4发生的过程:H2CrO4→Cr(OH)3中Cr元素化合价降低,因此H2CrO4作还氧化剂;
反应方程式为:2H2CrO4+3H2O2═2Cr(OH)3↓+3O2↑+2H2O,根据方程式可知:生成3mol气体转移6mol电子,则转移了0.3mol电子,则产生的气体的物质的量为
| 0.3 |
| 6 |
故答案为:H2CrO4和O2,3.36;
(4)①mg气体的物质的量=
| mg |
| Mg/mol |
| m |
| M |
| m |
| M |
| 2mNA |
| M |
故答案为:
| 2mNA |
| M |
②VL该气体的质量为
| V |
| 22.4 |
| VM |
| 22.4 |
| m溶质 |
| m溶液 |
| ||
|
| VM |
| VM+22400 |
故答案为:
| VM |
| VM+22400 |
点评:本题考查电离方程式的书写、电解质、非电解质及强弱电解质概念的辨析、氧化还原反应氧化剂、氧化产物及电子数的相关计算,以及物质的量和溶液质量分数的计算,题量较大,难度中等.

练习册系列答案
相关题目
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、2.24LH2含有的原子数为0.2NA |
| B、常温常压下,18gNH4+的电子数为10 NA |
| C、标准状况下,1NAH2O分子占有的体积约为22.4L |
| D、0.5 mol/L的AlCl3溶液中,Cl-的数目为1.5NA |
设NA 为阿伏加德罗常数的值.下列说法正确的是( )
| A、室温下,1LpH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA |
| B、0.1molMg在空气中完全燃烧生成MgO和Mg3N2,转移的电子数为0.2NA |
| C、标准状况下,22.4 L Cl2溶于足量NaOH溶液中,转移的电子数目为0.2NA |
| D、1 L 0.1 mol?L-1的Fe2(SO4)3溶液中,Fe3+的数目为0.2NA |
人们习惯上把金、银、铜、铁、锡五种金属统称为“五金”.在“五金”顺序中,把一种金属的位置向后移一位,正好符合某化学规律.这种金属和该化学规律是( )
| A、铁、金属活动性顺序表 |
| B、金、质量守恒定律 |
| C、银、元素周期律 |
| D、铜、金属密度顺序表 |
在一定温度和压强下,2体积X2气体与3体积Y2气体化合生成2体积气体化合物,则该化合物的化学式为( )
| A、XY3 |
| B、XY |
| C、X3Y2 |
| D、X2Y3 |

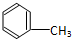 C:CH3CH2OH
C:CH3CH2OH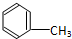 在浓硫酸作用下,与浓硝酸共热至100℃反应的化学方程式为:
在浓硫酸作用下,与浓硝酸共热至100℃反应的化学方程式为: