题目内容
10.已知298K时,CO2(g)的△H为-393.5kJ•mol-1,H2O(l)的△H=-285.8kJ•mol-1,乙炔的燃烧热为-1300kJ•mol-1,则乙炔的标准生成热为( )| A. | 227.2kJ•mol-1 | B. | -227.2kJ•mol-1 | C. | 798.8kJ•mol-1 | D. | -798.8kJ•mol-1 |
分析 由题给信息可知,①C(s)+O2 (g)=CO2 (g)△H=-393.5kJ/mol,②H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-285.8kJ/mol,③C2H2(g)+$\frac{5}{2}$O2 (g)=2CO2 (g)+H2O(l)△H=-1300kJ•mol-1,利用盖斯定理可得到2C(s)+H2(g)=C2H2(g)的反应热.
解答 解:由题给信息可知,①C(s)+O2 (g)=CO2 (g)△H=-393.5kJ/mol,②H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-285.8kJ/mol,③C2H2(g)+$\frac{5}{2}$O2 (g)=2CO2 (g)+H2O(l)△H=-1300kJ•mol-1,
则利用盖斯定理,将①×2+②-③可得2C(s)+H2(g)=C2H2(g)△H=2×(-393.5kJ/mol)+(-285.8kJ/mol)-(-1300kJ•mol-1)=+227.2kJ•mol-1,
故选A.
点评 本题考查了化学反应能量变化,为高频考点,侧重考查学生的分析能力和计算能力,注意把握燃烧热概念分析应用以及热化学方程式的计算等知识,注意盖斯定律的运用,题目较简单.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
20.下列说法正确的是( )
| A. | 硫酸的摩尔质量是98g | |
| B. | 1mol O2的质量是32g•mol-1 | |
| C. | 2g氢气含有氢原子的物质的量是2mol | |
| D. | 64g Fe的物质的量是1mol |
5.设NA为阿伏伽德罗常数值.下列有关叙述正确的是( )
| A. | 电解精炼粗铜(含有锌铁等杂质),若阳极溶解32g铜,转移电子数目为NA | |
| B. | 256gS8(分子结构如图)含S-S键数为7NA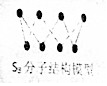 | |
| C. | 某温度下,pH=1的1LH2SO4溶液中含有的H+数目为0.1NA | |
| D. | 氢氧燃料电池正极消耗22.4L气体时,负极消耗的气体分子数目为2NA |
15.下列说法不正确的是( )
| A. | 用酚酞溶液可区别苯酚钠溶液与福尔马林 | |
| B. | 用溴水可区别丙烯与丙烯酸 | |
| C. | 用新制的Cu(OH)2悬浊液可区别醋酸与乙醇 | |
| D. | 无法用溴水除去苯中溶有的少量苯酚 |
2.甲物质与强碱溶液反应只生成盐和水,甲一定不属于( )
| A. | 酸 | B. | 盐 | C. | 金属单质 | D. | 氧化物 |
19.下列试剂保存方法正确的是( )
| A. | 氯水保存在棕色试剂瓶中 | |
| B. | 氢氧化钠溶液保存在带有玻璃塞的玻璃试剂瓶中 | |
| C. | 金属钠保存在水中 | |
| D. | 氢氟酸保存在玻璃试剂瓶中 |
8.下列离子化合物中,阴阳离子间的距离最大的是( )
| A. | LiCl | B. | NaCl | C. | KCl | D. | KBr |
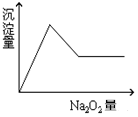 某溶液中可能含有下列8种离子中的一种或几种:H+、Na+、Cu2+、Mg2+、Al3+、NH4+、CO32-、Cl-.向该溶液中加入Na2O2固体放出一种无色无味的气体且产生白色沉淀,沉淀的量随加入Na2O2的量变化关系如图所示.试对该溶液中离子组成情况作出判断.
某溶液中可能含有下列8种离子中的一种或几种:H+、Na+、Cu2+、Mg2+、Al3+、NH4+、CO32-、Cl-.向该溶液中加入Na2O2固体放出一种无色无味的气体且产生白色沉淀,沉淀的量随加入Na2O2的量变化关系如图所示.试对该溶液中离子组成情况作出判断.